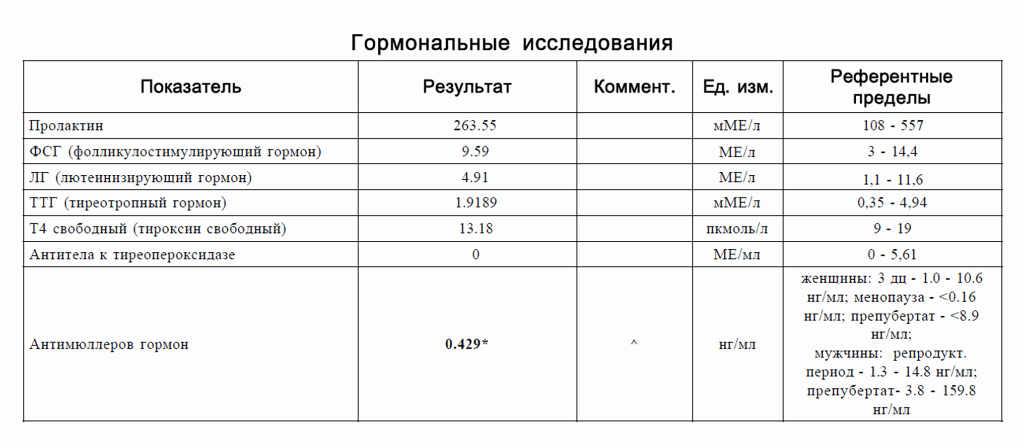
Антимюллеров гормон — что это такое, норма у женщин, таблица по возрасту, как правильно сдавать анализ, на какой день цикла, что делать, если повышен или понижен
Выяснить, что такое антимюллеров гормон, можно, если рассмотреть репродуктивную систему человека. Роль этого показателя очень важна в детородном возрасте, ведь он является отражением возможности выносить и родить здорового ребёнка.
Содержание записи:
Функции антимюллерова гормона в организме
АМГ вырабатывается организмом мужчин и женщин, место его появления – половые железы. Именно это вещество отвечает за половое развитие человека и возможность воспроизводить потомство. Несмотря на наличие гормона в мужском и женском организме, на схожие функции по установлению способности иметь детей, его функционирование различается.
Химия определяет антимюллеров гормон к группе протеиновых, отвечающих за клеточный рост. Вещество отвечает за контроль образования и роста фолликулов в женских яичниках. Именно они становятся яйцеклетками, которые ожидают оплодотворения сперматозоидами в полости матки.
Именно они становятся яйцеклетками, которые ожидают оплодотворения сперматозоидами в полости матки.
Функции АМГ:
- является фактором, обеспечивающим репродуктивную способность представителей обоих полов;
- в мужском организме он отвечает за создание наружных половых органов (происходит этот процесс ещё во время внутриутробного развития малыша). Нарушение этой функции влечёт за собой оставление в мужском организме женских половых органов или их части, а также способствует развитию крипторхизма и, даже мужского бесплодия, в будущем;
- в женском организме гормон начинает свою работу на последних неделях беременности, он обеспечивает способность без проблем зачать, выносить и родить здорового ребёнка. Пик выработки гормона приходится на 25 лет, к 50 годам – он прекращает продуцироваться организмом женщины;
- от работы и количества этого гормона зависит количество яйцеклеток, производимых женским организмом.
АМГ у мужчин и женщин: отличия
Мужской организм вырабатывает гормон АМГ наравне с женским, играя такую роль:
- Отвечает за формирование половых органов у мальчиков, которые могут полноценно работать и производить здоровых сперматозоидов.

- Первое время гормон вырабатывается материнским организмом, в детородном возрасте, эту функцию берёт на себя тело мальчика.
- В период полового созревания, количество вырабатываемых гормонов находится на низком уровне.
- Нарушение производства АМГ организмом мальчика, способно повлечь за собой нарушение правильной работы половых органов (неопущение одного или обоих яичек в мошонку), возникновения грыж паховой области.
- Неправильный уровень антимюллерова гормона влечёт за собой проблемы с репродуктивной системой молодого человека.
Женский организм тоже вырабатывает это вещество, причём на протяжении всей жизни меняется количественное значение этого показателя.
Роль АМГ в организме женщины выражается в следующем:
- Как и у мальчиков, АМГ впервые возникает в организме девочки в ходе внутриутробного развития.
- До тех пор, пока не наступил детородный возраст, уровень вещества имеет низкие значения. Только к 20 годам он существенно повышается.

- Низкий уровень гормона влечёт за собой проблемы с репродуктивным здоровьем, из-за того что фолликулы не позволяют созревать яйцеклеткам в нужном количестве.
- Расходование фолликулов, которые отмерены женщине на время детородного периода, влечёт за собой постепенное изменение гормонального уровня. АМГ в этот период, способен меняться в пределах от 5 до 20 нанограммов.
- Специалисты считают АМГ своеобразным маркером, который отмечает особенности репродуктивной системы женщины.
- Снижение уровня вещества в организме влечёт за собой спад способности женщины иметь детей.
Как вырабатывается АМГ?
Чтобы разобраться, антимюллеров гормон – что это такое, следует разобраться в процессе его выработки организмом человека.
Производством такого вещества занимаются половые железы:
- у мужчин: клетки Сертоли, которые находятся в яичках, в семенных каналах;
- у женщин: клетки, которые находятся в фолликулах, формируемых яичниками.

Выработка гормона имеет несколько этапов:
- До рождения.
- В период полового созревания у женщин (максимальная концентрация).
- После полового созревания (максимум у мужчин).
- На протяжении всей жизни (у мужчин угасает чуть раньше, у женщин к 50 годам, в период наступлении менопаузы).
Мюллеровы протоки — что это такое?
Мюллеровы протоки, находящиеся в тесной взаимосвязи с АМГ — это каналы, имеющие пару. Они образуются в организме человека ещё в первом триместре беременности, примерно на 8 неделе.
Особенности:
- в женском организме, такие протоки позже трансформируются в верхний свод влагалища, трубы матки и эпителий, выстилающий полость матки;
- в мужском организме – происходит их атрофия под действием соответствующего гормона, после чего они становятся маточкой простаты. Этот процесс длится на протяжении нескольких лет, пока не завершится процесс полового созревания. В случае внутриутробных нарушений, может возникать синдром персистенции, когда протоки не атрофируются, а формируют верх влагалища и фаллопиевые трубы.

В каких случаях назначается анализ?
Антимюллеров гормон, требует такого пристального внимания в разные периоды жизни людей, это тот показатель, который может показать, что не в порядке с органами и системами.
Его назначают в таких случаях:
- Если у мальчиков в возрасте до 12 лет, чаще 1 раза в год возникают паховые грыжи.
- Малышам в первый год жизни, в случае, когда наблюдается неопущение одного или обоих яичек в мошонку.
- Мужчинам в зрелом возрасте, при наличии бесплодия с неустановленными причинами.
- Для того чтобы установить настоящий пол человека, если по другим признаков определить это не представляется возможным.
- С целью диагностики у подростков и детей преждевременного полового созревания или его значительной задержки.
- Чтобы оценить способность женщины забеременеть.
- Для диагностики онкологических заболеваний женских половых органов.
- В случае нескольких неудачных попыток забеременеть при помощи ЭКО.

Подготовка и проведение анализа
Выяснив, что такое антимюллеров гормон, нужно выбрать правильный день для сдачи анализа на определение его уровня:
- мужчина может сдавать анализ в любой удобный для него день;
- уровень гормона у женщин меняется в тесной связи с менструальным циклом, но такие изменения очень незначительны, чаще всего доктора не требуют привязки к определённым периодам. Но, с целью получения достоверного результата, нужно сдавать анализ в период со 2 по 5 дни цикла. Это связано с пиковыми показателями гормонов, которые наблюдаются за 4 дня до и после предполагаемой овуляции.
Подготовка к забору крови выглядит таким образом:
- Сдача производится только натощак, в утреннее время. Причём время без пищи не должно составлять более 14 часов подряд.
- За 4 дня до сдачи крови не допускается употребление спиртных напитков.
- Не следует идти на анализ сразу же после выздоровления или при малейших признаках недомогания, лучше подождать 1-2 недели.

- Перед анализом не следует испытывать серьёзные физические нагрузки.
- Важно избегать стрессовых ситуаций.
- Сдача крови на уровень АМГ требует отказа на этот период от приёма других гормональных препаратов. В случае приёма стероидных или тиреоидных препаратов, следует за 2 суток отказаться от них.
- За час до анализа запрещается курить.
Для анализа происходит забор крови из вены. Уровень АМГ определяется при помощи специальной сыворотки. Результат готов в течение 2 суток.
Расшифровка результатов
Для применения результатов анализа в постановке правильного диагноза, требуется их грамотная расшифровка.
Нормы АМГ выглядят так:
- женщина детородного возраста, имеющая хорошее здоровье, чаще всего имеет уровень гормона в пределах 1-2,5 нанограмм на миллилитр. Превышение этих значений может являться свидетельством перенесённой антиандрогенной терапии, опухолевых образований органов малого таза, отсутствия овуляции, поликистоза яичников;
- мужские нормы находятся в пределах 5,98 нанограммов на миллилитр.
 Пониженное содержание гормона является признаком патологии яичек врождённого характера, влиянием возраста или опухолях яичек.
Пониженное содержание гормона является признаком патологии яичек врождённого характера, влиянием возраста или опухолях яичек.
Постановка верного диагноза возможна только после полного обследования организма. Специалист может предложить пересдачу анализа, для получения верных результатов, если существуют подозрения в неправильном заборе анализа.
Нормы АМГ: таблица
| Возраст | Величина (нанограмм/ миллилитр) | |
| Женщины | Мужчины | |
| Дети до 2 лет | До 5 | 15-500 |
| От 2 до 12 лет | До 10 | 7-240 |
| От 13 до 45 лет | 1-10 | 0,7-20 |
| Старше 45 лет | Менее 1 | 5-140 |
Причины повышения показателей
После определения показателя под названием антимюллеров гормон что это такое становится понятно, что теперь приходит очередь определить причины завышенных его показателей.
Выделяют 2 группы причин повышения АМГ:
- Когда фолликулы, имеющие показатели здоровых, не выходят из яичников. Поэтому не получают возможности быть оплодотворёнными. Подобная ситуация свойственна синдрому поликистозных яичников, когда развитый и выросший фолликул не может преодолеть поверхность с
Антимюллеровский гормон
Антимюллеровский гормон
Общая информация об исследовании
Антимюллеровский гормон (АМГ) в норме синтезируется только клетками Сертоли яичек (как в период эмбрионального развития, так и после рождения) и зернистыми клетками яичников (только после рождения). Он получил свое название благодаря уникальному свойству препятствовать развитию женских половых структур из зачатка, называемого Мюллеровым протоком. Хотя пол ребенка определяется в момент зачатия, до 6-й недели беременности плод имеет недифференцированные половые гонады и зачатки внутренних половых структур обоих полов: мезонефритический проток (Вольфов) и парамезонефритический проток (Мюллеров). Изначально плод развивается по женскому типу. При этом Мюллеров проток стимулирует развитие матки, маточных труб и верхней части влагалища, а клетки Вольфова протока разрушаются. И наоборот, при наличии подавляющих факторов разрушению подвергается Мюллеров проток, а Вольфов дает начало придатку яичка, семявыносящему каналу и семенным пузырькам – таким образом, развитие половой системы происходит по мужскому типу. Одним из таких факторов, в итоге анатомически формирующих мужской пол ребенка, является антимюллеровский гормон. Он вырабатывается клетками Сертоли яичка примерно с 7-й недели эмбрионального развития. Его основная функция – подавить формирование женских половых структур из мюллерова протока. Если у плода генетически мужского пола происходят мутации в гене антимюллеровского гормона или мутации в гене его рецептора, то развитие мюллерова протока продолжается и, наряду с внутренними мужскими половыми структурами, формируются и женские половые структуры (матка, маточные трубы или шейка матки).
Изначально плод развивается по женскому типу. При этом Мюллеров проток стимулирует развитие матки, маточных труб и верхней части влагалища, а клетки Вольфова протока разрушаются. И наоборот, при наличии подавляющих факторов разрушению подвергается Мюллеров проток, а Вольфов дает начало придатку яичка, семявыносящему каналу и семенным пузырькам – таким образом, развитие половой системы происходит по мужскому типу. Одним из таких факторов, в итоге анатомически формирующих мужской пол ребенка, является антимюллеровский гормон. Он вырабатывается клетками Сертоли яичка примерно с 7-й недели эмбрионального развития. Его основная функция – подавить формирование женских половых структур из мюллерова протока. Если у плода генетически мужского пола происходят мутации в гене антимюллеровского гормона или мутации в гене его рецептора, то развитие мюллерова протока продолжается и, наряду с внутренними мужскими половыми структурами, формируются и женские половые структуры (матка, маточные трубы или шейка матки).
Другой важной функцией АМГ является опускание яичек из полости живота в мошонку. При отклонении АМГ опускание яичек нарушено. Задержка опускания яичек (крипторхизм) – самая частая патология мочеполовой системы у мальчиков, она встречается у 30 % недоношенных и у 5 % доношенных детей. Как правило, опускание яичек все же происходит спонтанно к 3-му месяцу жизни. Если этого не случается к 6 месяцам, выполняется операция по перемещению яичек из полости живота или пахового канала в мошонку (орхидопексия). У большинства пациентов с недостатком или нечувствительностью к АМГ наблюдается крипторхизм, так что им назначают такую операцию. Часто именно во время орхидопексии обнаруживают дополнительные внутренние женские половые структуры и предполагают синдром персистирующего Мюллерова протока.
Врачи, наблюдающие мальчика с крипторхизмом, сталкиваются с определенными трудностями. Такая патология может встречаться как при нарушении опускания яичек, так и при их отсутствии. У этих отклонений совершенно разный прогноз и лечение, поэтому необходима их правильная дифференциальная диагностика. Ультразвуковое исследование позволяет выявить тестикулярную ткань в полости живота или пахового канала лишь в 70-80 % случаев, в то время как АМГ является специфическим (98 %) и чувствительным (91 %) индикатором наличия тестикулярной ткани. Положительный тест на АМГ у мальчика свидетельствует о нарушении опускания яичек, что может быть скорректировано с помощью операции. Отсутствие АМГ позволяет диагностировать анорхию (врождённое двустороннее отсутствие яичек), при которой операция не показана. В связи с этим измерение АМГ может быть использовано для дифференциальной диагностики крипторхизма.
Концентрация АМГ значительно изменяется в течение жизни. Уровень АМГ у мальчика низкий при рождении, но значительно повышается к 6 месяцам. В детском и подростковом возрасте АМГ постепенно снижается и достигает самых низких значений во взрослой жизни. В отличие от новорождённых мальчиков, уровень АМГ у младенцев женского пола в норме очень низкий (не определяется) и остается таким в детском и подростковым периоде. Во время полового созревания у девочек он незначительно повышается и в течение взрослой жизни соответствует таковому у взрослых мужчин. Уровень АМГ после менопаузы в норме не определяется. Таким образом, концентрации АМГ у мальчиков и девочек в период новорождённости и раннего детства значительно отличаются, поэтому АМГ может быть использован для диагностики синдромов нарушения дифференцировки пола. При наличии у младенца наружных половых структур, обладающих как женскими, так и мужскими признаками, АМГ в сочетании с некоторыми другими показателями позволяет не только определить истинный пол, но и выявить причину нарушения дифференцировки пола.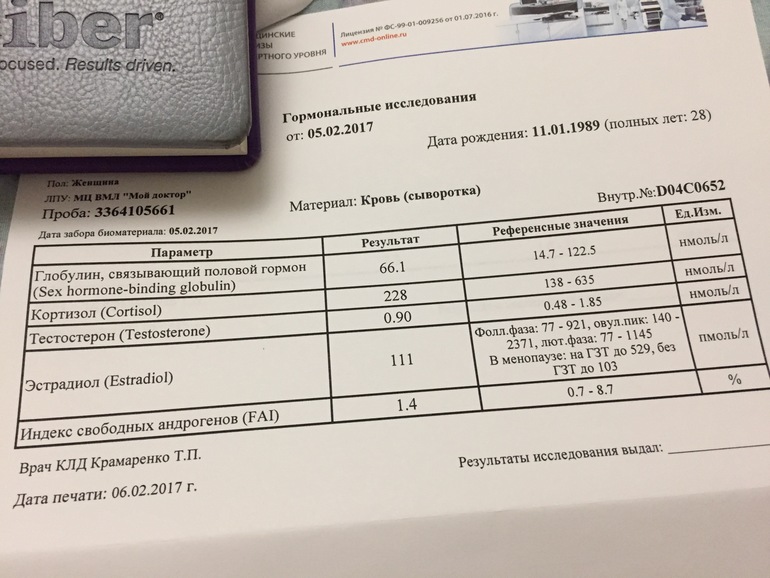
Несмотря на то что главная функция АМГ реализуется при развитии зародыша, этот гормон осуществляет ряд задач и после рождения. В организме взрослого мужчины он участвует в регуляции синтеза андрогенов. Уровень сывороточного АМГ у мужчин с необструктивной азооспермией (отсутствие сперматозоидов в эякуляте из-за их нарушенного образования) на 50 % ниже, чем у пациентов с обструктивной азооспермией (отсутствие сперматозоидов в эякуляте из-за препятствия в семявыводящих протоках). Данный лабораторный показатель является даже более точным методом дифференциальной диагностики двух вариантов азооспермии, чем традиционно применяемый анализ на фолликулостимулирующий гормон (ФСГ), поэтому АМГ может быть использован для выявления причины мужского бесплодия.
Данный лабораторный показатель является даже более точным методом дифференциальной диагностики двух вариантов азооспермии, чем традиционно применяемый анализ на фолликулостимулирующий гормон (ФСГ), поэтому АМГ может быть использован для выявления причины мужского бесплодия.
В организме женщины АМГ участвует в созревании фолликулов, а также их отборе для овуляции. Он синтезируется зернистыми клетками растущих фолликулов, подавляет рост соседних примордиальных фолликулов, а также уменьшает чувствительность растущих фолликулов к действию ФСГ. Все это способствует окончательному созреванию и овуляции одного фолликула каждый месяц. Так как синтез АМГ осуществляется растущими фолликулами, по его концентрации оценивают их количество. В свою очередь, количество растущих фолликулов отражает количество покоящихся примордиальных фолликулов, которые называют функциональным резервом яичников. Этот резерв снижается с возрастом, а также при состояниях, сопровождающихся преждевременной менопаузой (например, при химиотерапии). Оценка функционального резерва с помощью АМГ позволяет ответить на многие вопросы. Достаточно часто современная женщина сознательно откладывает рождение ребенка. При этом доказано, что вероятность зачатия первого ребенка в течение 1 года женщиной старше 31 года уменьшается в 6 раз по сравнению с более молодыми женщинами. К 41 году количественные и качественные изменения фолликулов в подавляющем большинстве случаев приводят к так называемой естественной инфертильности, причем она наступает гораздо раньше, чем менопауза. Поэтому оценка функционального резерва яичников позволяет определить примерный возраст наступления менопаузы и инфертильности (бесплодия), что может быть учтено молодыми женщинами при планировании беременности. Низкий уровень АМГ указывает на наступление менопаузы в ближайшие 5 лет. Преимущества теста на АМГ в том, что концентрация этого гормона не изменяется значительно в течение менструального цикла, а также остается постоянной от одного цикла к другому.
Оценка функционального резерва с помощью АМГ позволяет ответить на многие вопросы. Достаточно часто современная женщина сознательно откладывает рождение ребенка. При этом доказано, что вероятность зачатия первого ребенка в течение 1 года женщиной старше 31 года уменьшается в 6 раз по сравнению с более молодыми женщинами. К 41 году количественные и качественные изменения фолликулов в подавляющем большинстве случаев приводят к так называемой естественной инфертильности, причем она наступает гораздо раньше, чем менопауза. Поэтому оценка функционального резерва яичников позволяет определить примерный возраст наступления менопаузы и инфертильности (бесплодия), что может быть учтено молодыми женщинами при планировании беременности. Низкий уровень АМГ указывает на наступление менопаузы в ближайшие 5 лет. Преимущества теста на АМГ в том, что концентрация этого гормона не изменяется значительно в течение менструального цикла, а также остается постоянной от одного цикла к другому.
Оценка функционального резерва яичников с помощью АМГ также производится при отборе и подготовке пациенток к программам экстракорпорального оплодотворения для лечения женского бесплодия.
АМГ является маркером опухолей яичников, происходящих из зернистых клеток (гранулезоклеточных опухолей). На их долю приходится около 3 % новообразований яичников. Чаще встречается так называемый взрослый вариант опухоли, наблюдающийся у женщин в пре- и постменопаузе (средний возраст, в котором диагностируется опухоль, – 51 год). При этом наряду с повышенной продукцией АМГ значительно увеличивается количество эстрогенов, что приводит к гиперплазии эндометрия, которая проявляется нарушениями менструального цикла в пременопаузальном периоде.
Повторные анализы на АМГ могут быть использованы на этапе контроля за лечением опухолей.
Для чего используется исследование?
- Для дифференциальной диагностики причин крипторхизма: задержки опускания яичек или анорхии (а также синдрома персистирующего Мюллерова протока).
- Для диагностики нарушения дифференцировки пола и выявления его причины.
- Для диагностики необструктивной азооспермии как причины мужского бесплодия.
- Чтобы оценить функциональный резерв яичников в целях планирования беременности и прогнозирования срока наступления менопаузы.
- Чтобы выделить группы пациенток с недостаточным или избыточным ответом на стимуляцию овуляции при проведении программ экстракорпорального оплодотворения и коррекции лечения женского бесплодия.

- Для диагностики гранулезоклеточных опухолей яичников и яичек и контроля за их лечением, а также для диагностики новообразований из клеток Сертоли.
Когда назначается исследование?
- При крипторхизме – отсутствии яичек в мошонке у новорождённого мальчика.
- При наличии у новорождённого наружных половых структур, обладающих как женскими, так и мужскими признаками.
- При дифференциальной диагностике обструктивной и необструктивной азооспермии.
- Когда прогнозируют возраст наступления инфертильности и менопаузы.
- При выделении групп пациенток: а) с недостаточным ответом на стимуляцию овуляции и неблагоприятным прогнозом наступления беременности; б) с избыточным ответом на стимуляцию овуляции и неблагоприятным прогнозом развития синдрома гиперстимуляции яичников.
- При симптомах гиперэстрогенизма у женщин (маточное кровотечение) и у мужчин (гинекомастия).
что это такое, можно ли забеременеть при пониженном уровне
Антимюллеров гормон играет важную роль в организме женщины. Это органический продукт, который продуцируют специальные клетки яичников, его уровень меняется в период полового созревания, а при наступлении климакса сводится к нулю. Если антимюллеров гормон понижен, можно ли забеременеть? Этот вопрос волнует многих женщин.
Это органический продукт, который продуцируют специальные клетки яичников, его уровень меняется в период полового созревания, а при наступлении климакса сводится к нулю. Если антимюллеров гормон понижен, можно ли забеременеть? Этот вопрос волнует многих женщин.
…
Вконтакте
Мой мир
Что это такое
АМГ гормон – что это такое? Он начинает вырабатываться у девочек с момента рождения. Как только девушка начинает менструировать, его уровень увеличивается.Максимальная концентрация АМГ у женщин наблюдается в возрастном промежутке от 20 до 30 лет, именно поэтому эти 10 лет считаются наиболее благоприятными для рождения ребенка.
Антимюллеров гормон влияет на половое созревание и способность зачать ребенка. Особенность в том, что его уровень целиком зависит от функционирования яичников, продуцирование АМГ не контролирует головной мозг.
По этой причине у девочек этот органический продукт присутствует в неизменном количестве до начала полового созревания. В период пременопаузы, в возрасте 40–45 лет, выработка АМГ снижается, происходит изменение гормонального фона, и у женщины наступает климакс. Кроме этого, низкое содержание органического продукта в крови значительно понижает способность к зачатию.
Антимюллеров гормон отвечает за функционирование фолликулов и количество зрелых яйцеклеток, кроме этого, эстроген полностью зависит от АМГ. Он оказывает влияние на формирование женских половых органов эмбриона, от его уровня зависит, как сформируется матка, придатки и влагалище девочки.
Норма АМГ у женщин
Показатель нормы у женщин данного вещества полностью зависит от возраста и внешних факторов. Если антимюллеров гормон повышен, многие пары не могут зачать ребенка и вынуждены прибегать к ЭКО. Для планирования беременности необходим АМГ анализ.
Нормальные показатели:
- девочки – 1,8–3.
 4 нг/мл;
4 нг/мл; - женщины репродуктивного возраста (норма для зачатия) – 2,1–7,2 нг/мл;
- норма для климакса – 0–1,1 нг/мл.
Количественный показатель данного вещества может колебаться в зависимости от особенностей организма или наличия патологий репродуктивной системы. У некоторых в 50 лет АМГ вырабатывается больше, чем у молодой девушки в возрасте 25 лет.
Обратите внимание! Продуцирование этого органического вещества не зависит ни от менструального цикла женщины, ни от ее рациона питания.
Анализ для определения уровня антимюллерова гормона назначается женщинам, которые не могут забеременеть, или при планировании зачатия с помощью ЭКО.
Анализ на АМГ
Анализ крови можно сдать только в условиях клиники; чтобы получить результат, достаточно двух часов. Кроме ситуаций, когда возникает проблема с наступлением беременности, сдавать антимюллеров гормон рекомендуют в диагностических целях. Показанием являются следующие состояния:
- отмечены нарушения в период полового созревания у девочек;
- подозревается бесплодие неясной этиологии;
- значительно повышен уровень гормона, стимулирующего фолликулы;
- при наступлении ранней менопаузы или нарушении менструального цикла;
- при неудачных процедурах ЭКО.

- после перенесенной болезни инфекционного характера кровь нужно сдавать не ранее чем через две недели с момента выздоровления;
- исключить стрессовые ситуации и повышенные физические нагрузки за 2–3 дня до забора крови;
- перед сдачей анализа ни в коем случае не следует курить;
- употребление алкоголя необходимо прекратить за 5 суток до сдачи крови;
- анализ сдается натощак, можно пить только воду.
По одному АМГ анализу не всегда можно определить причину отклонений от нормы, но все же он является достаточно информативным. По результату можно отследить динамику снижения запаса женских яйцеклеток и заморозить материал в целях будущего оплодотворения.
Причины отклонения от нормы
В норме уровень вещества в крови снижается после 45 лет.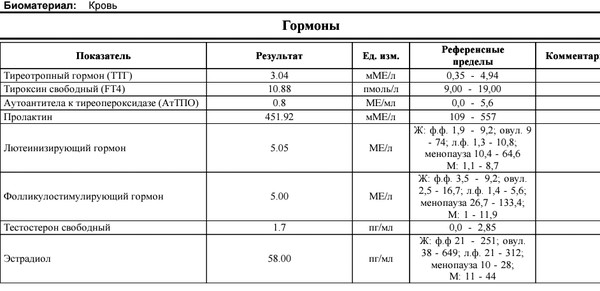 Если это произошло раньше, причиной могут быть следующие патологии:
Если это произошло раньше, причиной могут быть следующие патологии:
- половое созревание наступило раньше времени;
- преждевременный климакс;
- женское бесплодие;
- малое количество яйцеклеток в яичниках;
- механические травмы;
- лишний вес на фоне эндокринных нарушений.
Важно! Низкий уровень при беременности опасен тем, что ребенок может родиться гермафродитом, с половыми признаками и мальчика, и девочки.
Для того чтобы не допустить развития патологии, пациентке прописывается гормональная заместительная терапия с целью устранения причины отклонения и нормализации гормонального уровня.
Если антимюллеров гормон повышен (превышает показатель 7,2 нг/мл), причиной отклонения могут стать следующие факторы:
- повышенная физическая нагрузка, обусловленная условиями труда или спортивными тренировками;
- позднее половое созревание;
- состояние постоянного стресса, страха;
- злоупотребление алкоголем, курением, наркотиками в период беременности и зачатия ребенка;
- патологическое отсутствие овуляции на генетическом уровне;
- кисты яичников;
- опухоли яичников доброкачественного или злокачественного характера.

Для снижения продуцирования АМГ применяют медикаментозное лечение, предварительно проведя полное диагностическое обследование. На протяжении всего курса лечения пациентка должна соблюдать полный покой и категорически избегать стрессов.
Если терапия по устранению бесплодия не принесла результата, женщину могут направить на искусственное оплодотворение.
Как повысить уровень АМГ
Многие женщины интересуются, смогут ли они забеременеть, если уровень АМГ понижен.Низкий АМГ не исключает такую возможность, но шансы значительно уменьшаются. Если анализ показал отклонение от нормы в меньшую сторону, женщину направляют на ЭКО.
Уровень АМГ не оказывает влияния на саму возможность иметь детей, беременность может наступить и при отклонениях.
Гормон – это индикатор патологий. Диагноз бесплодие ставится только при очень низком показателе.
Не менее важен вопрос о том, как повысить антимюллеров гормон у женщин. Медикаментозно это сделать невозможно, необходимо устранять причину, которая спровоцировала отклонение от нормы. Ни в коем случае нельзя этим заниматься самостоятельно, необходима помощь квалифицированного специалиста.
Ни в коем случае нельзя этим заниматься самостоятельно, необходима помощь квалифицированного специалиста.
Считается, что можно повысить гормон у женщин народными средствами, используя в качестве пищевых добавок продукты пчеловодства. Они оказывают общеукрепляющее действие и улучшают лактацию, но нет никаких доказательств, что они повышают уровень АМГ. Необходимо периодически сдавать анализ крови в целях контроля репродуктивной функции и своевременного устранения первопричины отклонений.
Норма АМГ для зачатия
Нормальным уровнем, при котором возможно зачатие, считается показатель 2,0-7,2 нг/мл. Для определения возможности забеременеть необходима стимуляция яичников, в результате которой должны выработаться здоровые яйцеклетки, способные к оплодотворению. Низкий АМГ и ответ яичников на стимуляцию считаются показаниями для искусственного оплодотворения. Фолликулярный запас невозможно нормализовать никакими средствами. Чаще всего такой результат обусловлен следующими факторами:
- пациентка старше 40-45 лет;
- объем яичников < 3 см3;
- каждый яичник содержит < 5 антральных фолликулов на 3 день менструального цикла;
- фолликулостимулирующий гормон понижен;
- перенесенная операция на яичниках;
- курс химио- или лучевой терапии.

В этом случае желанная беременность может не наступить даже в результате процедуры ЭКО.
Что такое биостерон
Биостерон или дегидроэпиандростерон – это стероид широкого спектра действия, считается гормоном молодости.Применяется для нормализации гормонального фона и укрепления иммунитета, не считается лекарством. Перед применением лучше проконсультироваться с врачом.
Прием начинается с малых доз, которые постепенно увеличиваются.
Чтобы улучшить качество яйцеклеток женщинам после 40 лет рекомендуемый курс – три раза в день по 25 мг в течение трех месяцев, с наступлением беременности прием препарата следует прекратить. Необходимо помнить, что ДГЭА имеет внушительный список противопоказаний и побочных эффектов.
Важно! Биостерон категорически нельзя применять при наличии опухолевых процессов в организме и пациентам, находящимся в группе риска развития онкологии.
Видео: роль АМГ, норма в крови
Вывод
Уровень антимюллерова гормона в крови можно изменить, когда причиной отклонения стал стресс или развитие патологии. Женщина проходит курс лечения, и со временем АМГ может нормализоваться. Если отклонение является врожденным, изменить гормональный уровень невозможно. Поэтому в целях планирования беременности необходимо следить за показателями гормонального фона.
Вконтакте
Одноклассники
Мой мир
Антимюллеров гормон, что это такое у женщин и мужчин
Формирование репродуктивной системы у эмбриона по женскому или мужскому типу, сперматогенез, созревание фолликулов – все эти функции выполняет антимюллеров гормон. В медицинской литературе встречается несколько названий этого вещества: антимюллеровый, антимюллеров, антимюллеровский гормон, употребляется его сокращенное наименование – АМГ.
АМГ и репродуктивная система человека
Вырабатывается биологически активное вещество у представителей обоих полов. У женщин гормон производится первичными фолликулами, у мужчин – клетками Сертоли, яичками. В отличее от других гормонов, секреция АМГ практически не контролируется головным мозгом.
Гормон АМГ влияет на формирование тканей развивающегося организма. Особую роль это вещество играет при закладке и развитии репродуктивной системы человека. На начальных этапах индивидуального развития установить половую принадлежность нормального эмбриона невозможно.
Ранний зародыш имеет как женское начало (мюллеровы протоки), так и мужское (вольфовы протоки). В ходе дальнейшего развития зародыша антимюллеровый гормон имеет определяющее значение в формировании женских и мужских половых органов.
Назначение мюллеровских протоков – формирование репродуктивной системы по женскому типу, так как из них развиваются матка, маточные трубы и другие женские половые органы.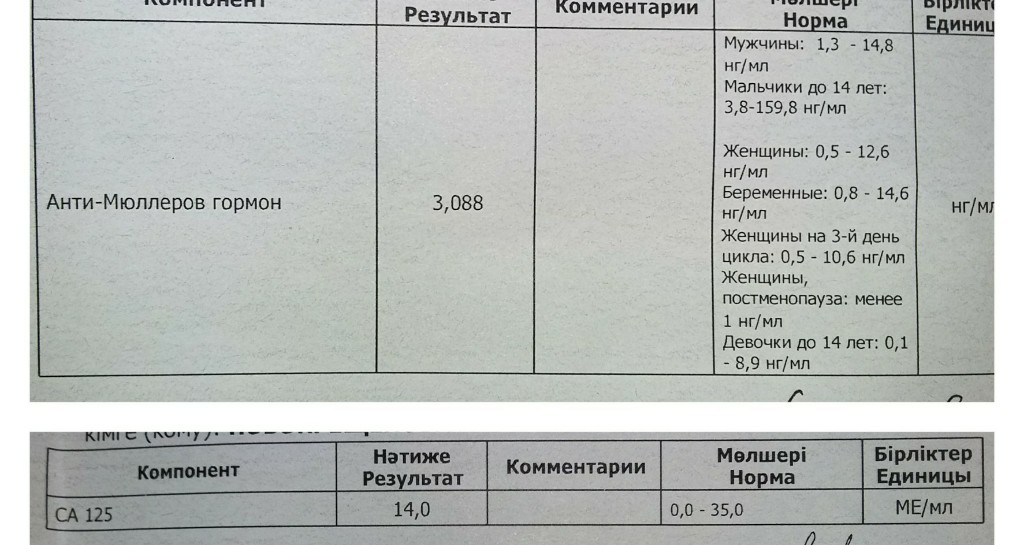
Чтобы началось формирование мужских половых органов, мюллеровские протоки необходимо разрушить. Именно эту задачу и выполняет антимюллеров гормон (АМГ). Его концентрация у эмбрионов мужского пола повышается уже с 8 недели внутриутробного развития.
Далее действие вещества направлено на формирование полноценных мужских половых органов. После рождения у младенца мужского пола продолжается синтез антимюллерова гормона тестикулами (яичками) до начала пубертатного периода. Недостаточная концентрация вещества у мальчиков приводит к серьезным проблемам:
- яички не опускаются в мошонку,
- вероятно развитие паховой грыжи,
- гермафродитизм ложного типа,
- нарушение детородной функции.
АМГ у мужчин в зрелом возрасте присутствует в небольшом количестве. И тем не менее, играет важную роль в процессах зачатия ребенка, так как влияет на процесс сперматогенеза.
У женщин АМГ ведет себя иначе. Его синтез тоже начинается еще в ходе внутриутробного развития. С момента рождения и до начала периода полового созревания у девочек количество этого вещества незначительное. С началом полового созревания и до наступления первых признаков угасания репродуктивной функции, связанных с менопаузой, ситуация кардинально меняется.
С момента рождения и до начала периода полового созревания у девочек количество этого вещества незначительное. С началом полового созревания и до наступления первых признаков угасания репродуктивной функции, связанных с менопаузой, ситуация кардинально меняется.
Уровень АМГ в течение этого продолжительного периода жизни женщины остается довольно высоким. Антимюллеров гормон у женщин имеет определяющее значение в созревании фолликулов, наступлении овуляции, создании условий для оплодотворения. Непосредственно на зачатие он не оказывает влияния, это скорее индикатор состояния репродуктивного здоровья женщины
Вещество присутствует в организме представителей обоих полов и очень важен для выполнения репродуктивной функции. Расшифровка анализа на количество АМГ позволяет установить:
- количественные характеристики овариального резерва,
- наличие онкологии яичников,
- качественные характеристики сперматогенеза.

Анализ на определение концентрации АМГ назначается, если у молодых людей детородного возраста возникли проблемы с зачатием ребенка, необходимо выявление причин бесплодия, есть необходимость подтверждения диагноза, связанного с онкологическими заболеваниями.
Повышенное содержание
Повышенный АМГ гормон свидетельствует:
- о задержке полового развития у юноши,
- о проявлении крипторхизма (расположение яичка вне мошонки),
- о наличии поликистоза или опухоли яичников,
- о гонадотропной недостаточности.
Пониженное содержание
Причинами повышенного уровня гормона являются:
- гонадотропный гипогонадизм,
- избыточный вес,
- недоразвитие половых желез (яичек или яичников),
- преждевременное созревание женщины,
- менопауза и климакс,
- генетические нарушения.
Антимюллеров гормон и беременность
Низкая концентрация антимюллерова гормона в организме женщине может стать причиной нарушения детородной функции. Малые показатели АМГ связаны с количеством половых клеток у женщины. Гормон образно называют «счетчиком яйцеклеток»
Малые показатели АМГ связаны с количеством половых клеток у женщины. Гормон образно называют «счетчиком яйцеклеток»
Несмотря на то, что уровень АМГ не зависит от количества других гормонов, для определения шансов на зачатие следует провести тщательное исследование гормонального фона. Гормонов, отвечающих за формирование женской клетки и овуляцию, несколько: эстрогены, прогестерон, лютенизирующий, фолликулостимулирующий.
Например, процесс выхода зрелой жизнеспособной яйцеклетки обеспечивается соотношением антимюллерова и фолликулостимулирующего гормона (ФСГ). При допустимом соотношении низкого АМГ и ФСГ высокого, зачатие возможно с большой долей вероятности. В медицинской практике описаны случаи, когда у женщин случались выкидыши при низких показателях АМГ. Стоит отметить, что уровень этого вещества с самопроизвольным абортом никак не связан.
При невысоких показателях АМГ в гинекологии используется методика стимуляции яичников для получения здоровых яйцеклеток. В дальнейшем они используются для проведения оплодотворения и вынашивания с применением альтернативных способов.
В дальнейшем они используются для проведения оплодотворения и вынашивания с применением альтернативных способов.
Низкий показатель антимюллерова гормона может быть свидетельством патологических процессов в организме. При их устранении нормальные показатели вещества восстанавливаются.
Антимюллеров гормон и ЭКО
Процедура экстракорпорального оплодотворения позволяет провести процесс слияния зрелой яйцеклетки и жизнеспособного сперматозоида в пробирке. Через 2-5 дней полученный зародыш переносят в полость матки. Антимюллеров гормон не влияет на процесс прикрепления и дальнейшее внутриутробное развитие эмбриона.
Для проведения процедуры нужно получить здоровую яйцеклетку. Низкая и высокая концентрация вещества оказывает негативное влияние на стимуляцию яичников. При недостаточном количестве вещества не удается получить зрелые яйцеклетки. Собранные клетки не готовы к оплодотворению (оно не наступает или ткани эмбриона делятся неправильно).
При высоком уровне АМГ наблюдается опасное состояние – гиперстимуляция яичников. Это может привести к отеку, нарушению кровообращения органов малого таза и представлять угрозу для жизни пациентки.
Это может привести к отеку, нарушению кровообращения органов малого таза и представлять угрозу для жизни пациентки.
Антимюллеров гормон имеет определяющее значение в формировании половой принадлежности у эмбриона. Его уровень довольно высокий у мальчиков до полового созревания, что указывает на значимость вещества в процессе правильного формирования и функционирования половых органов у будущего мужчины. У женщин уровень гормона резко повышается только с момента полового созревания. Он является показателем состояния ее репродуктивной системы и возможности стать матерью.
Загрузка…Антимюллеров гормон – что это такое у женщин
Содержание статьи:
Репродуктивная функция женского организма напрямую зависит от работы половых гормонов. Они способствуют созреванию яйцеклетки в полости яичников. Благодаря этому в определенный период времени наступает процесс оплодотворения.
Эти вещества помогают контролировать обменные реакции и человеческом организме. Неправильная работа половых желез может стать причиной бесплодия.
Неправильная работа половых желез может стать причиной бесплодия.
Для чего нужен данный гормон
Правильное планирование беременности подразумевает исследование уровня антимюллерова гормона. Он представляет собой белковую молекулу, которая выделяется как женским, так и мужским организмом.
В данном случае оптимальный уровень этого вещества у женщин помогает подготовить органы малого таза к вынашиванию плода.
Антимюллеров гормон отвечает за образование здоровых и полноценных яйцеклеток. Данную молекулу вырабатывают яичники. На начальном этапе пубертатного периода его уровень достигает максимального значения.
По мере роста женского организма он начинает постепенно снижаться. В период климакса выработка гормона полностью прекращается.
Своевременная сдача анализа помогает контролировать процесс созревания яйцеклеток. Если продуцирование белковой молекулы (АМГ) резко сокращается, то данное явление провоцирует наступление сбоев в менструальном цикле.
В результате это может стать причиной преждевременного бесплодия среди женщин репродуктивного возраста.
В отличие от фолликуллостимулирующих и лютеинзирующих молекул контролировать продуцирование антимюллерова гормона невозможно при помощи медикаментозной терапии. Его значения напрямую зависят от первоначального запаса яйцеклеток в полости яичников.
Показания для сдачи анализа на АМГ
Проводить подобное медицинское исследование, рекомендуется на первоначальном этапе планирования беременности. Для этого врач назначает сдачу развёрнутого анализа крови на запас антимюллерова гормона.
Существует ряд медицинских показаний, которые требуют данного обследования. К ним относят:
- длительное отсутствие оплодотворения яйцеклеток;
- самопроизвольное прерывание беременности после нескольких попыток ЭКО;
- изменения в строении яичников;
- ранее бесплодие;
- высокие показатели фолликулярного гормона в составе крови;
- подозрение на гранулёзоклеточные типы опухолей;
- длительное отсутствие полового созревания у девочек.
Перед взятием биоматериала, рекомендуется пройти соответствующую подготовку. Она включает в себя следующие требования:
- за 2 суток запрещено употреблять спиртосодержащие напитки;
- перед сдачей крови необходимо избегать нервного напряжения;
- последний прием пищи и жидкости осуществляют за 13 часов до взятия биологического материала.
Нормы и отклонения уровня АМГ
В организме каждой женщины наблюдают идентичный уровень яйцеклеток. Уровень антимюллерова гормона также отличается. В каждом возрасте наблюдают его изменения. В результате этого в некоторых случаях отмечают появление беременности в возрасте 35 – 45 лет. В других она отсутствует на протяжении всей жизни.
Сокращение фолликулов в молодом возрасте провоцирует преждевременное бесплодие, которое не поддается медицинскому лечению.
Средние показатели АМГ в женском организме (НГ/мл) достигают следующих показателей:
- до 11 лет от 1,6 до 3,5;
- с 11 до 20 лет от 2 до 6,5;
- с 20 до 35 лет от 3,5 до 7;
- с 35 до 60 лет от 6,5 до 2,5
- период климакса от 2,5 до;
- возраст более 65 лет от 1 до 0.
Динамика изменений показателей АМГ
В медицине выделяют динамичное изменение содержания АМГ гормона в составе яичников. По статистике этот процесс происходит в следующей очередности:
- у девочек в возрасте 10 лет он начинает постепенно увеличиваться;
- в 20 – 35 лет уровень антимюллерова гормона достигает максимальных значений;
- после 35 лет выработка белковых молекул сокращается в несколько раз;
- в период менопаузы и климакса значения АМГ снижаются до 0. В это время выработка яйцеклеток полностью отсутствует.
О чем говорит повышенный уровень АМГ?
Выделяют ряд причин, по которым диагностируют высокий уровень АМГ в женском организме. К ним относят:
- патологические процессы в тканях яичников;
- раковые новообразования в области малого таза;
- инфекционные и венерические заболевания;
- поликистоз;
- гиперстимуляция медицинскими препаратами.Данное мероприятие используют для образования преждевременной овуляции;
- длительное отсутствие пубертатного периода.
Чрезмерное количество антимюллерова гормона свидетельствует о серьезных патологических процессах в районе детородных органов. Своевременная диагностика помогает предотвратить преждевременное бесплодие у женщин.
Антимюллеров гормон — Anti-Müllerian hormone
Антимюллер гормон ( АМГ ), также известные как Мюллеровый ингибирующий гормон (MIH), представляет собой гликопротеин , гормон , структурно связан с ингибиной и активином от фактора роста бета трансформирующего надсемейства, чьи ключевых роли в дифференциации и роста фолликулогенезе . У людей ген AMH — это AMH на хромосоме 19p 13.3, а ген AMHR2 кодирует свой рецептор на хромосоме 12 .
АМГ активируется SOX9 в клетках Сертоли мужского плода. Его экспрессия подавляет развитие женских половых путей или Мюллерова протоков ( парамезонефрических протоков ) у мужского эмбриона , тем самым останавливая развитие маточных труб, матки и верхних отделов влагалища. Экспрессия AMH имеет решающее значение для дифференциации пола в определенное время во время развития плода и, по-видимому, жестко регулируется ядерным рецептором SF-1 , факторами транскрипции GATA , геном изменения пола DAX1 и фолликулостимулирующим гормоном (FSH). Было показано, что мутации как в гене AMH, так и в рецепторе AMH типа II вызывают сохранение производных Мюллера у мужчин, которые обычно маскулинизируются.
АМГ также является продуктом гранулезных клеток преантральных и малых антральных фолликулов у женщин. Таким образом, AMH присутствует только в яичниках до наступления менопаузы. Продукция AMH регулирует фолликулогенез путем ингибирования рекрутирования фолликулов из пула в состоянии покоя для выбора доминирующего фолликула, после чего производство AMH уменьшается. Являясь продуктом гранулезных клеток, которые обволакивают каждое яйцо и снабжают его энергией, АМГ также может служить молекулярным биомаркером относительного размера резерва яичников . У людей это полезно, потому что количество клеток в фолликулярном резерве можно использовать для прогнозирования времени наступления менопаузы. У крупного рогатого скота AMH можно использовать для отбора самок в программах переноса многоовуляторных эмбрионов путем прогнозирования количества антральных фолликулов, развившихся до овуляции. АМГ также может использоваться в качестве маркера дисфункции яичников, например, у женщин с синдромом поликистозных яичников (СПКЯ).
Структура
АМГ представляет собой димерный гликопротеин с молярной массой 140 кДа . Молекула состоит из двух идентичных субъединиц, связанных сульфидными мостиками, и характеризуется N-концевым димером (про-областью) и C-концевым димером. AMH связывается со своим рецептором типа 2 AMHR2 , который фосфорилирует рецептор типа I по сигнальному пути TGF beta .
Функция
Эмбриогенез
У самцов млекопитающих AMH предотвращает развитие мюллерова протоков в матку и другие мюллеровы структуры. Эффект является ипсилатеральным, то есть каждое яичко подавляет развитие Мюллера только на своей стороне. У людей это действие происходит в течение первых 8 недель беременности. Если половые железы не производят гормонов, автоматически развиваются мюллеровы протоки, а вольфовы протоки , отвечающие за мужские репродуктивные органы, автоматически умирают. Количества AMH, которые можно измерить в крови, зависят от возраста и пола. АМГ работает, взаимодействуя со специфическими рецепторами на поверхности клеток тканей-мишеней ( рецепторами антимюллерова гормона ). Наиболее известный и наиболее специфический эффект, опосредованный рецепторами AMH типа II, включает запрограммированную гибель клеток ( апоптоз ) ткани-мишени (мюллеровы протоки плода).
Яичников
АМГ выражается зернистыми клетками из яичника в течение репродуктивного периода, и ограничивает образование первичных фолликулов путем ингибирования чрезмерного фолликулярного набора ФСГА. Экспрессия AMH максимальна на стадии рекрутирования фолликулогенеза в преантральных и малых антральных фолликулах. Эта экспрессия уменьшается по мере развития фолликулов и перехода на стадию отбора, после которой экспрессия ФСГ увеличивается. Некоторые авторитетные источники полагают, что это мера определенных аспектов функции яичников, полезная при оценке таких состояний, как синдром поликистозных яичников и преждевременная недостаточность яичников .
Другой
Продукция AMH клетками Сертоли семенников остается высокой в детстве у мужчин, но снижается до низких уровней в период полового созревания и взрослой жизни. Было показано, что АМГ регулирует выработку половых гормонов , и изменение уровня АМГ (повышение у женщин, падение у мужчин) может быть связано с наступлением половой зрелости у обоих полов. Также было обнаружено, что функциональные рецепторы AMH экспрессируются в нейронах мозга эмбриональных мышей и, как полагают, играют роль в половом диморфном развитии мозга и последующем развитии гендерно-специфического поведения.
Патология
У мужчин неадекватная эмбриональная активность AMH может привести к синдрому стойкого мюллерова протока (PMDS), при котором присутствует рудиментарная матка и яички обычно не опущены . Ген AMH ( AMH ) или ген его рецептора ( AMH-RII ) обычно не соответствует норме. Измерения AMH также стали широко использоваться для оценки наличия и функции яичек у младенцев с интерсексуальными состояниями, неоднозначными гениталиями и крипторхизмом .
Исследование, опубликованное в журнале Nature Medicine, обнаружило связь между гормональным дисбалансом в матке и синдромом поликистозных яичников (СПКЯ), в частности пренатальным воздействием антимюллерова гормона. Для исследования исследователи вводили беременным мышам АМГ, чтобы у них была концентрация гормона выше нормы. Действительно, они родили дочерей, у которых позже развились склонности к СПКЯ. К ним относятся проблемы с фертильностью, задержка полового созревания и беспорядочная овуляция. Чтобы обратить вспять, исследователи вводили поликистозным мышам препарат для ЭКО под названием цетрореликс , который заставил симптомы исчезнуть. Эти эксперименты должны быть подтверждены на людях, но они могут стать первым шагом к пониманию взаимосвязи между поликистозом яичников и антимюллеровым гормоном.
Уровни в крови
У здоровых женщин АМГ либо просто обнаруживается, либо не обнаруживается в пуповинной крови при рождении и демонстрирует заметный рост к трехмесячному возрасту; хотя он все еще обнаруживается, он падает до четырехлетнего возраста, а затем линейно возрастает до восьмилетнего возраста, оставаясь довольно постоянным с середины детства до раннего взросления — он существенно не изменяется в период полового созревания . Рост в детстве и подростковом возрасте, вероятно, отражает разные стадии развития фолликулов. С 25 лет АМГ снижается до неопределяемого уровня в период менопаузы.
Стандартное измерение AMH соответствует анализу поколения II . Это должно дать те же значения, что и в ранее используемом анализе IBC, но значения AMH из ранее использованного анализа DSL следует умножить на 1,39, чтобы соответствовать текущим стандартам, поскольку в нем использовались другие антитела.
Слабые данные свидетельствуют о том, что АМГ следует измерять только на ранней фолликулярной фазе из-за изменений в менструальном цикле . Кроме того, уровень АМГ снижается при текущем использовании оральных контрацептивов и курении табака .
Референсные диапазоны
Референсные диапазоны для антимюллерова гормона, по оценкам референтных групп в США , следующие:
Самки:
| Возраст | Единица измерения | Ценность |
|---|---|---|
| Моложе 24 месяцев | нг / мл | Менее 5 |
| пмоль / л | Менее 35 | |
| От 24 месяцев до 12 лет | нг / мл | Менее 10 |
| пмоль / л | Менее 70 | |
| 13–45 лет | нг / мл | От 1 до 10 |
| пмоль / л | От 7 до 70 | |
| Более 45 лет | нг / мл | Менее 1 |
| пмоль / л | Менее 7 |
Самцы:
| Возраст | Единица измерения | Ценность |
|---|---|---|
| Моложе 24 месяцев | нг / мл | От 15 до 500 |
| пмоль / л | От 100 до 3500 | |
| От 24 месяцев до 12 лет | нг / мл | От 7 до 240 |
| пмоль / л | От 50 до 1700 | |
| Более 12 лет | нг / мл | 0,7 до 20 |
| пмоль / л | От 5 до 140 |
Измерения АМГ могут быть менее точными, если у человека, которого измеряют, наблюдается дефицит витамина D. Обратите внимание, что мужчины рождаются с более высоким уровнем АМГ, чем женщины, чтобы инициировать половую дифференциацию, а у женщин уровни АМГ снижаются со временем по мере снижения фертильности.
Клиническое использование
Общая оценка фертильности
Сравнение индивидуального уровня АМГ со средними уровнями полезно при оценке фертильности, поскольку оно дает представление о резерве яичников и выявляет женщин, которым, возможно, придется рассмотреть возможность замораживания яйцеклеток или попытки забеременеть раньше, чем позже, если у них есть долгосрочные будущая рождаемость оставляет желать лучшего. Было обнаружено, что более высокий уровень антимюллерова гормона у женщин в общей популяции имеет положительную корреляцию с естественной фертильностью у женщин в возрасте 30–44 лет, стремящихся к спонтанному зачатию, даже после поправки на возраст. Однако эта корреляция не была обнаружена в сопоставимом исследовании более молодых женщин (в возрасте от 20 до 35 лет).
Экстракорпоральное оплодотворение
АМГ является предиктором ответа яичников при экстракорпоральном оплодотворении (ЭКО). Измерение АМГ поддерживает клинические решения, но само по себе не является подходящим предиктором успеха ЭКО. Кроме того, уровни АМГ используются для оценки оставшегося количества яйцеклеток у женщины.
Согласно NICE руководящих принципов по ин витро оплодотворения , анти-мюллеровой уровень гормона меньше или равна 5,4 пмоль / л (0,8 нг / мл) предсказывает низкий ответ на гиперстимуляции яичников , в то время как более высокий уровень , чем или равно 25,0 пмоль / l (3,6 нг / мл) прогнозирует высокий ответ. Другие пороговые значения, найденные в литературе, варьируются от 0,7 до 20 пмоль / л (от 0,1 до 2,97 нг / мл) для слабого ответа на гиперстимуляцию яичников. Следовательно, более высокие уровни АМГ связаны с большей вероятностью живорождения после ЭКО, даже с поправкой на возраст. Таким образом, АМГ можно использовать для рационализации программы индукции овуляции и принятия решений о количестве эмбрионов для переноса в методах вспомогательной репродукции, чтобы максимизировать показатели успешности беременности и минимизировать риск синдрома гиперстимуляции яичников (СГЯ). AMH может прогнозировать чрезмерный ответ при гиперстимуляции яичников с чувствительностью и специфичностью 82% и 76% соответственно.
Измерение одного только АМГ может ввести в заблуждение, поскольку высокие уровни возникают при таких состояниях, как синдром поликистозных яичников, и поэтому уровни АМГ следует учитывать в сочетании с трансвагинальным сканированием яичников для оценки количества антральных фолликулов и объема яичников.
Природные средства
Исследования методов лечения низкого резерва яичников и низкого уровня АМГ увенчались успехом. На сегодняшний день наилучшие имеющиеся данные свидетельствуют о том, что ДГЭА улучшает функцию яичников, увеличивает шансы на беременность и, уменьшая анеуплоидию, снижает частоту выкидышей. Исследования DHEA при низком уровне АМГ показывают, что следует принимать дозу 75 мг в течение 16 недель. Улучшение качества ооцитов / эмбрионов с помощью добавок DHEA потенциально предполагает новую концепцию старения яичников, при которой стареет среда яичников, но не сами ооциты. ДГЭА дает положительные результаты для женщин с уровнем АМГ более 0,8 нг / мл или 5,7 пмоль / л. ДГЭА не оказывает видимого воздействия на ооциты или среду яичников в этом диапазоне.
Исследования добавок CoQ10 на модели пожилых животных замедлили истощение резерва яичников, восстановили экспрессию митохондриальных генов ооцитов и улучшили митохондриальную активность. Авторы отмечают, что повторение 12–16 недель использования добавок CoQ10 на мышах для достижения этих результатов было бы эквивалентно десятилетию у людей.
Считается, что витамин D играет роль в регуляции АМГ. Промотор гена AMH содержит элемент ответа на витамин D, который может влиять на уровень витамина D в сыворотке крови. Женщины с уровнем витамина D 267,8 ± 66,4 нмоль / л демонстрируют в 4 раза больший успех при процедуре ЭКО, чем женщины с низким уровнем 104,3 ± 21 нмоль / л. При определении сывороточного уровня АМГ для диагностики следует учитывать дефицит витамина D.
Женщины с раком
У женщин с раком лучевая терапия и химиотерапия могут повредить яичниковый резерв. В таких случаях предварительное лечение АМГ полезно для прогнозирования долгосрочной потери функции яичников после химиотерапии, что может указывать на стратегии сохранения фертильности, такие как криоконсервация ооцитов . АМГ после лечения связан со снижением фертильности.
Гранулезно-клеточные опухоли яичника секретируют АМГ, и тест на АМГ имеет чувствительность от 76 до 93% при диагностике таких опухолей. АМГ также полезен при диагностике рецидивов опухолей гранулезных клеток.
Статус стерилизации у животных
В ветеринарии измерения AMH используются для определения статуса стерилизации самцов и самок собак и кошек. Уровни АМГ также можно использовать для диагностики синдрома остаточного яичника.
Биомаркер синдрома поликистозных яичников
Синдром поликистозных яичников (СПКЯ) — это эндокринное заболевание, наиболее часто встречающееся у женщин репродуктивного возраста, которое характеризуется олиго- или ановуляцией , гиперандрогенизмом и поликистозом яичников (СПКЯ). Это эндокринное заболевание увеличивает уровень AMH почти в два-три раза у женщин с СПКЯ, чем у женщин с нормальным типом. Это часто связывают с увеличением количества фолликулов, характерным для СПКЯ, что указывает на увеличение количества клеток гранулезы, поскольку они окружают каждую отдельную яйцеклетку. Однако повышенный уровень АМГ также объясняется не только увеличением количества фолликулов, но и повышенным количеством АМГ, продуцируемого одним фолликулом. Высокий уровень андрогенов, характерный для СПКЯ, также стимулирует и обеспечивает обратную связь для увеличения производства АМГ. Таким образом, AMH все чаще рассматривается как инструмент или биомаркер, который можно использовать для диагностики или индикации СПКЯ.
Биомаркер синдрома Тернера
Синдром Тернера является наиболее распространенным наследственным заболеванием, связанным с половыми хромосомами у женщин во всем мире, с частотой 1 случая на 2000 живорождений. Одним из важных патологических признаков является преждевременная недостаточность яичников, приводящая к аменорее или даже бесплодию. Специалисты рекомендовали регулярно контролировать фолликулостимулирующий гормон и ингибин B, чтобы оценить состояние яичников. В последнее время несколько исследователей рекомендуют антимюллеров гормон в качестве более точного биомаркера развития фолликулов. Биологическая функция антимюллерова гормона в яичниках состоит в том, чтобы противодействовать рекрутированию примордиальных фолликулов, запускаемому ФСГ, сохраняя пул фолликулов для дальнейшего рекрутирования и овуляции. Когда наступает менопауза, у нормальных женщин концентрация антимюллерова гормона в сыворотке крови почти не определяется. Таким образом, вариации уровней АМГ в детстве могут теоретически предсказать продолжительность репродуктивной жизни любой данной девочки, предполагая, что скорость непрерывной потери фолликулов сопоставима между людьми.
Возможное использование в будущем
Был синтезирован АМГ. Его способность подавлять рост тканей, происходящих из мюллерова протоков, породила надежды на полезность при лечении различных заболеваний, включая эндометриоз , аденомиоз и рак матки . Исследования ведутся в нескольких лабораториях. Если были более стандартизированы AMH анализы, потенциально могут быть использованы в качестве биомаркеров от синдрома поликистозных яичников .
Было показано, что у мышей увеличение AMH уменьшает количество растущих фолликулов и, следовательно, общий размер яичников. Это увеличение продукции АМГ уменьшает первичные, вторичные и антральные фолликулы без уменьшения количества примордиальных фолликулов, что свидетельствует о блокаде активации примордиальных фолликулов. Это может обеспечить жизнеспособный метод контрацепции, который защищает яичниковый резерв ооцитов во время химиотерапии, не извлекая их из организма, обеспечивая возможность естественного воспроизводства в более позднем возрасте.
Имена
Прилагательное «Müllerian» пишется либо «Müllerian» , либо «Müllerian» , в зависимости от руководства по стилю ; производный термин с префиксом « анти- » означает «антимюллеровский», «антимюллерский» или «антимюллерский». Мюллеровы каналы названы в честь Иоганнеса Петера Мюллера .
Список названий, которые использовались для антимюллерова гормона, следующий. Для простоты в этом списке игнорируются некоторые орфографические вариации; например, он дает только одну строку для «гормона, ингибирующего Мюллериан», хотя есть 4 приемлемых его стиля (заглавная буква M или строчная буква m, дефис или пробел).
| Укладка имени белка | Символ белка |
|---|---|
| Антимюллеров гормон | AMH |
| Мюллерова-ингибирующий фактор | МИФ |
| Гормон, ингибирующий Мюллериан | MIH |
| Вещество, ингибирующее Мюллериан | MIS |
| Фактор ингибирования Мюллерова протока | MDIF |
| Фактор регрессии Мюллера | MRF |
| Антипарамезонефрический гормон | APH |
Смотрите также
Ссылки
Антимюллеров гормон — Infogalactic: ядро планетарных знаний
Антимюллеров гормон , также известный как AMH — это белок, который у людей кодируется геном AMH . [1] Он подавляет развитие мюллерова протоков (парамезонефрических протоков) у мужского эмбриона. [2] Его также называют Мюллерово-ингибирующий фактор (MIF), Мюллерово-ингибирующий гормон (MIH), Мюллерово-ингибирующее вещество (MIS) и Антипарамезонефрический гормон (APH). [3] Назван в честь Иоганнеса Петера Мюллера.
Хотя рецептор AMH экспрессируется как у плодов мужского, так и женского пола, экспрессия AMH была выделена в мужских клетках Сертоли. [4] Экспрессия AMH активируется SOX9 в мужских клетках сертоли и вызывает необратимую регрессию мюллерова протоков. [5] Поскольку экспрессия AMH имеет решающее значение для дифференциации пола в определенное время во время развития плода, она, по-видимому, жестко регулируется факторами SF1, GATA, DAX1 и FSH. [6] [7] [8] Было показано, что мутации как в гене AMH, так и в рецепторе AMH типа II вызывают сохранение производных Мюллера у мужчин, которые обычно вирилизованы. [9]
ЭкспрессияAMH также наблюдается в клетках гранулезы яичников женщин в послеродовом периоде и служит молекулярным биомаркером относительного размера резерва яичников. [10] У людей количество клеток в фолликулярном резерве можно использовать для прогнозирования времени наступления менопаузы. [11] У крупного рогатого скота AMH может использоваться для отбора самок в программах многоовуляторного переноса эмбрионов путем прогнозирования количества антральных фолликулов, развившихся до овуляции. [12]
Распространение видов
AMH присутствует у рыб, рептилий, птиц, сумчатых и плацентарных млекопитающих. [ требуется ссылка ]
Источники
AMH секретируется клетками Сертоли семенников во время эмбриогенеза плода мужского пола. У женщин он секретируется клетками гранулезы фолликулов яичников.
Конструкция
AMH представляет собой белковый гормон, структурно связанный с ингибином и активином, и член семейства трансформирующих факторов роста-β (TGF-β). Это димерный гликопротеин. Он имеет молярную массу 140 кДа. [13]
Джин
У человека ген AMH AMH на хромосоме 19p13.3, [1] , тогда как ген AMHR2 кодирует свой рецептор на хромосоме 12. [14]
Функция
Эмбриогенез
У млекопитающих AMH предотвращает развитие мюллерова протоков в матку и другие мюллеровы структуры. [2] Эффект ипсилатеральный, то есть каждый семенник подавляет развитие Мюллера только на своей стороне. [15] У человека это действие происходит в течение первых 8 недель беременности. Если половые железы не производят гормонов, автоматически развиваются мюллеровы протоки, а вольфовы протоки, отвечающие за мужские репродуктивные части, автоматически умирают. [16] Количества AMH, которые можно измерить в крови, зависят от возраста и пола. AMH работает, взаимодействуя со специфическими рецепторами на поверхности клеток тканей-мишеней.Наиболее известный и наиболее специфический эффект, опосредованный рецепторами AMH типа II, включает запрограммированную гибель клеток (апоптоз) ткани-мишени (мюллеровы протоки плода).
Яичников
АМГ экспрессируется клетками гранулезы яичника в репродуктивном возрасте и ограничивает образование первичных фолликулов, подавляя чрезмерное рекрутирование фолликулов ФСГ. [10] [17] Некоторые авторитетные источники полагают, что это средство измерения определенных аспектов функции яичников, [18] полезно при оценке таких состояний, как синдром поликистозных яичников и преждевременная недостаточность яичников. [19] Полезно предсказать плохой ответ яичников при оплодотворении in vitro (ЭКО), но, по-видимому, не добавляет какой-либо прогнозной информации об успешности уже установленной беременности после ЭКО. [20] Кроме того, уровни АМГ используются для определения оставшегося количества яйцеклеток у женщин. [21]
Другое
ПродукцияAMH клетками Сертоли семенников остается высокой на протяжении всего детства у мужчин, но снижается до низких уровней в период полового созревания и взрослой жизни.Было показано, что АМГ регулирует выработку половых гормонов, [22] и изменение уровня АМГ (повышение у женщин, падение у мужчин) может быть связано с началом полового созревания у обоих полов. Было обнаружено, что функциональные рецепторы AMH экспрессируются на нейронах мозга эмбриональных мышей и, как полагают, играют роль в половом диморфном развитии мозга и последующем развитии гендерно-специфического поведения. [23]
Патология
У мужчин неадекватная эмбриональная активность AMH может привести к синдрому персистирующего мюллерова протока (PMDS), при котором присутствует рудиментарная матка и яички обычно не опущены.Ген AMH ( AMH ) или ген его рецептора ( AMH-RII ) обычно не соответствует норме. Измерения AMH также стали широко использоваться для оценки наличия и функции яичек у младенцев с интерсексуальными состояниями, неоднозначными гениталиями и крипторхизмом.
Уровни в крови
У здоровых женщин AMH либо просто обнаруживается, либо не обнаруживается в пуповинной крови при рождении и демонстрирует заметный рост к трехмесячному возрасту; хотя он все еще обнаруживается, он падает до четырехлетнего возраста, а затем линейно возрастает до восьмилетнего возраста, оставаясь довольно постоянным с середины детства до раннего взросления — он существенно не изменяется в период полового созревания. [24] Рост в детском и подростковом возрасте, вероятно, отражает разные стадии развития фолликулов. [17] С 25 лет АМГ снижается до неопределяемого уровня в период менопаузы. [24]
Стандартное измерение AMH соответствует тесту Generation II . Это должно дать те же значения, что и в ранее используемом анализе IBC, но значения AMH из ранее использованного анализа DSL следует умножить на 1,39, чтобы соответствовать текущим стандартам, поскольку в нем использовались другие антитела. [25]
Слабые данные свидетельствуют о том, что АМГ следует измерять только на ранней фолликулярной фазе из-за изменений в менструальном цикле. Кроме того, уровень АМГ снижается при текущем использовании оральных контрацептивов и курении табака. [26]
Референсные диапазоны
Референсные диапазоны для антимюллерова гормона, по оценкам референтных групп в США, следующие: [27]
Женщины:
| Возраст | Блок | Значение |
|---|---|---|
| Моложе 24 месяцев | нг / мл | Менее 5 |
| пмоль / л | Менее 35 | |
| от 24 месяцев до 12 лет | нг / мл | Менее 10 |
| пмоль / л | Менее 70 | |
| 13–45 лет | нг / мл | от 1 до 10 |
| пмоль / л | от 7 до 70 | |
| Более 45 лет | нг / мл | Менее 1 |
| пмоль / л | Менее 7 |
Мужчины:
| Возраст | Блок | Значение |
|---|---|---|
| Моложе 24 месяцев | нг / мл | от 15 до 500 |
| пмоль / л | от 100 до 3500 | |
| от 24 месяцев до 12 лет | нг / мл | от 7 до 240 |
| пмоль / л | 50 до 1700 | |
| Более 12 лет | нг / мл | 0.С 7 по 20 |
| пмоль / л | 5 до 140 |
Измерения АМГ могут быть менее точными, если у человека, у которого проводятся измерения, наблюдается дефицит витамина D. [28]
Клиническое применение
Экстракорпоральное оплодотворение
В соответствии с рекомендациями NICE по экстракорпоральному оплодотворению уровень антимюллерова гормона меньше или равен 5,4 пмоль / л (0,8 нг / мл) предсказывает слабый ответ на гиперстимуляцию яичников, в то время как уровень выше или равен 25.0 пмоль / л (3,6 нг / мл) означает высокий ответ. [29] Другие пороговые значения, найденные в литературе, варьируются от 0,7 до 20 пмоль / л (0,1 и 2,97 нг / мл) для слабого ответа на гиперстимуляцию яичников. [25] Следовательно, более высокие уровни АМГ связаны с большей вероятностью живорождения после ЭКО, даже с поправкой на возраст. [26] [30] AMH, таким образом, можно использовать для рационализации программы индукции овуляции и принятия решений о количестве эмбрионов для переноса в методах вспомогательной репродукции, чтобы максимизировать показатели успешности беременности при минимальном риске синдрома гиперстимуляции яичников (СГЯ). ) [31] [32] AMH может предсказать чрезмерный ответ при гиперстимуляции яичников с чувствительностью и специфичностью 82% и 76% соответственно. [33]
Измерение одного только AMH может ввести в заблуждение, поскольку высокие уровни возникают при таких состояниях, как синдром поликистозных яичников, и поэтому уровни AMH следует рассматривать в сочетании с трансвагинальным сканированием яичников для оценки количества антральных фолликулов [34] и объема яичников. [35]
Общая оценка фертильности
Сравнение индивидуального уровня АМГ со средними уровнями [24] также полезно при оценке фертильности, поскольку оно дает представление о резерве яичников и выявляет женщин, которым, возможно, придется рассмотреть возможность замораживания яйцеклеток или попытки забеременеть раньше. чем позже, если их фертильность в долгосрочной перспективе будет низкой. [36] Было обнаружено, что более высокий уровень антимюллерова гормона при тестировании у женщин в общей популяции имеет положительную корреляцию с естественной фертильностью у женщин в возрасте 30–44 лет, стремящихся к спонтанному зачатию, даже с поправкой на возраст. [26] Однако эта корреляция не была обнаружена в сопоставимом исследовании молодых женщин (в возрасте от 20 до 35 лет). [26]
Больные раком
У онкологических женщин лучевая терапия и химиотерапия могут повредить яичниковый резерв.В таких случаях предварительное лечение AMH полезно для прогнозирования долгосрочной потери функции яичников после химиотерапии, что может указывать на стратегии сохранения фертильности, такие как криоконсервация ооцитов. [26] АМГ после лечения ассоциируется со снижением фертильности. [17] [26]
Гранулезно-клеточные опухоли яичника секретируют АМГ, и чувствительность теста на АМГ при диагностике таких опухолей составляет от 76 до 93%. [26] AMH также полезен при диагностике рецидивов опухолей гранулезных клеток. [26]
Возможное использование в будущем
СинтезированАМГ. Его способность подавлять рост тканей, происходящих из мюллерова протоков, породила надежды на полезность при лечении различных заболеваний, включая эндометриоз, аденомиоз и рак матки. Исследования ведутся в нескольких лабораториях. Если бы существовали более стандартизованные анализы AMH, его можно было бы использовать в качестве биомаркера синдрома поликистозных яичников. [37]
См. Также
Список литературы
- ↑ 1.0 1,1 Кейт Р.Л., Матталиано Р.Дж., Хессион С, Тизард Р., Фарбер Н.М., Чунг А., Нинфа Е.Г., Фрей А.З., Гаш DJ, Чоу EP (июнь 1986 г.). «Выделение бычьих и человеческих генов для вещества, ингибирующего Мюллериан, и экспрессию человеческого гена в клетках животных». Ячейка . 45 (5): 685–98. DOI: 10.1016 / 0092-8674 (86)-X. PMID 3754790.
- ↑ 2,0 2.1 Behringer RR (1994). «Роли вещества, ингибирующего мюллериан, in vivo». Текущие темы биологии развития . Актуальные темы биологии развития. 29 : 171–87. DOI: 10.1016 / S0070-2153 (08) 60550-5. PMID 7828438.
- ↑ Минкофф Э., Бейкер П. (2004). Биология сегодня: подход к проблемам (Третье изд.). Нью-Йорк: Наука Гарланд. п. 296. ISBN 1136838759 .
- ↑ Рей Р., Лукас-Круазье С., Ласала С., Бедекаррас П. (декабрь 2003 г.). «AMH / MIS: что мы уже знаем о гене, белке и его регуляции». Молекулярная и клеточная эндокринология . 211 (1–2): 21–31. DOI: 10.1016 / j.mce.2003.09.007. PMID 14656472.
- ↑ Тагучи О, Кунья Г.Р., Лоуренс В.Д., Роббой С.Дж. (декабрь 1984 г.).«Время и необратимость ингибирования Мюллерова протока в эмбриональном репродуктивном тракте мужчины». Биология развития . 106 (2): 394–8. DOI: 10.1016 / 0012-1606 (84)
-0. PMID 6548718. - ↑ Шен WH, Мур CC, Икеда Y, Паркер KL, Ingraham HA (июнь 1994). «Ядерный рецептор стероидогенного фактора 1 регулирует ген ингибитора мюллерова вещества: связь с каскадом определения пола». Ячейка . 77 (5): 651–661. DOI: 10.1016 / 0092-8674 (94) -7. PMID 8205615.
- ↑ Nachtigal MW, Hirokawa Y, Enyeart-VanHouten DL, Flanagan JN, Hammer GD, Ingraham HA (май 1998 г.). «Опухоль Вильмса 1 и Dax-1 модулируют орфанный ядерный рецептор SF-1 в экспрессии генов, специфичных для пола». Ячейка . 93 (3): 445–454. DOI: 10.1016 / s0092-8674 (00) 81172-1. PMID 95
. - ↑ Viger RS, Mertineit C, Trasler JM, Nemer M (июль 1998 г.). «Фактор транскрипции GATA-4 экспрессируется по половому диморфному паттерну во время развития гонад у мышей и является мощным активатором промотора вещества, ингибирующего Мюллера». Развитие . 125 (14): 2665–2675. PMID 9636081.
- ↑ Белвилл К., Джоссо Н., Пикард Дж. Й. (декабрь 1999 г.).«Стойкость мюллерова производных у мужчин». Американский журнал медицинской генетики . 89 (4): 218–223. DOI: 10.1002 / (sici) 1096-8628 (19991229) 89: 4 <218 :: aid-ajmg6> 3.0.co; 2-е. PMID 10727997.
- ↑ 10,0 10,1 Weenen C, Laven JS, Von Bergh AR, Cranfield M, Groome NP, Visser JA, Kramer P, Fauser BC, Themmen AP (февраль 2004 г.). «Паттерн экспрессии анти-Мюллерова гормона в яичниках человека: потенциальные последствия для начального и циклического набора фолликулов». Молекулярная репродукция человека . 10 (2): 77–83. DOI: 10,1093 / мольхр / gah015. PMID 14742691.
- ↑ ван Дисселдорп Дж., Фэдди MJ, Themmen AP, de Jong FH, Peeters PH, van der Schouw YT, Broekmans FJ (июнь 2008 г.). «Взаимосвязь концентрации антимюллерова гормона в сыворотке с возрастом в период менопаузы». Журнал клинической эндокринологии и метаболизма . 93 (6): 2129–34.DOI: 10.1210 / jc.2007-2093. PMID 18334591.
- ↑ Rico C, Médigue C, Fabre S, Jarrier P, Bontoux M, Clément F, Monniaux D (март 2011). «Регулирование производства антимюллерова гормона у коров: многомасштабное исследование на эндокринных, яичниковых, фолликулярных и гранулезных уровнях». Биология репродукции . 84 (3): 560–571. DOI: 10.1095 / биолрепрод.110.088187. PMID 21076084.
- ↑ [1] Хампл Р., Шнайдерова М., Мардешич Т. (2011). «Антимюллеров гормон (АМГ) не только маркер для прогнозирования овариального резерва». Физиологические исследования / Academia Scientiarum Bohemoslovaca . 60 (2): 217–223. PMID 21114374.
- ↑ Имбо С., Фор Э, Ламар I, Маттеи М.Г., ди Клементе Н., Тизард Р., Карре-Эузеб Д., Бельвиль С., Трагетон Л., Тонкин С., Нельсон Дж., МакОлифф М., Бидар Дж. М., Лабабиди А., Джоссо Н. , Кейт Р.Л., Пикард Д.Ю. (декабрь 1995 г.).«Нечувствительность к антимюллеровому гормону из-за мутации человеческого рецептора антимюллерова гормона». Nature Genetics . 11 (4): 382–8. DOI: 10,1038 / NG1295-382. PMID 7493017.
- ↑ Стр. 1114 в: Уолтер Ф., PhD. Бор (2003). Медицинская физиология: клеточный и молекулярный подход . Elsevier / Saunders. п. 1300. ISBN 1-4160-2328-3 .
- ↑ Введение в поведенческую эндокринологию, Рэнди Дж. Нельсон, 3-е издание, Sinauer
- ↑ 17,0 17,1 17,2 Dewailly D, Andersen CY, Balen A, Broekmans F, Dilaver N, Fanchin R, Griesinger G, Kelsey TW, La Marca A, Lambalk C, Mason H, Nelson SM, Visser JA, Уоллес WH, Андерсон RA (2014). «Физиология и клиническое применение антимюллеровского гормона у женщин». Обновление репродукции человека . 20 (3): 370–385. DOI: 10.1093 / humupd / dmt062. PMID 24430863.
- ↑ Broer SL, Eijkemans MJ, Scheffer GJ, van Rooij IA, de Vet A, Themmen AP, Laven JS, de Jong FH, Te Velde ER, Fauser BC, Broekmans FJ (август 2011 г.). «Антимюллеров гормон предсказывает менопаузу: долгосрочное последующее исследование у нормовулятивных женщин». Журнал клинической эндокринологии и метаболизма . 96 (8): 2532–9.DOI: 10.1210 / jc.2010-2776. PMID 21613357.
- ↑ Visser JA, de Jong FH, Laven JS, Themmen AP (январь 2006 г.). «Антимюллеров гормон: новый маркер функции яичников». Репродукция . 131 (1): 1–9. DOI: 10.1530 / rep.1.00529. PMID 16388003.
- ↑ Broer SL, van Disseldorp J, Broeze KA, Dolleman M, Opmeer BC, Bossuyt P, Eijkemans MJ, Mol BW, Broekmans FJ (2013).«Дополнительная ценность тестирования яичникового резерва на характеристиках пациенток в прогнозировании ответа яичников и продолжающейся беременности: индивидуальный подход к данным пациента». Обновление репродукции человека . 19 (1): 26–36. DOI: 10.1093 / humupd / dms041. PMID 23188168.
- ↑ Индихова Дж. «Означает ли низкий уровень АМГ (антимюллерова гормона) бесплодие?». http: //www.fertileheart.com . Проверено 6 февраля 2015 г.
- ↑ Трбович А.М., Мартинель Н., О’Нил Ф.Х., Пирсон Э.Д., Донахью П.К., Слюсс П.М., Тейшейра Дж. (Октябрь 2004 г.). «Стероидогенная активность в клетках Лейдига MA-10 по-разному изменяется под действием цАМФ и вещества, ингибирующего Мюллериан». Журнал биохимии стероидов и молекулярной биологии . 92 (3): 199–208. DOI: 10.1016 / j.jsbmb.2004.07.002.PMID 15555913.
- ↑ Ван П.Ю., Протеро А., Кларксон А.Н., Имхофф Ф., Койши К., МакЛеннан И.С. (апрель 2009 г.). «Вещество, ингибирующее Мюллериан, способствует предубеждениям, связанным с полом, в мозгу и поведении». Труды Национальной академии наук Соединенных Штатов Америки . 106 (17): 7203–8. DOI: 10.1073 / pnas.0
3106. PMC 2678437. PMID 19359476. - ↑ 24,0 24,1 24,2 He H, Yu FX, Sun C, Luo Y (2011). Vitzthum VJ (ред.). «CBP / p300 и SIRT1 участвуют в регуляции транскрипции гистоновых генов, специфичных для S-фазы». PloS One . 6 (7): e22024. DOI: 10.1371 / journal.pone.0022024. PMC 3137624. PMID 21789216.
- ↑ 25,0 25.1 La Marca A, Sunkara SK (2013). «Индивидуализация контролируемой стимуляции яичников при ЭКО с использованием маркеров резерва яичников: от теории к практике». Обновление репродукции человека . 20 (1): 124–40. DOI: 10.1093 / humupd / dmt037. PMID 24077980.
- ↑ 26,0 26,1 26,2 26,3 26,4 26,5 26,6 26.7 Broer SL, Broekmans FJ, Laven JS, Fauser BC (2014). «Антимюллеров гормон: исследование резерва яичников и его потенциальные клинические последствия». Обновление репродукции человека . 20 (5): 688–701. DOI: 10,1093 / humupd / dmu020. PMID 24821925.
- ↑ Для значений массы: Для молярных значений: получено из значений массы с использованием 140 000 г / моль, как указано в:
- [2] Хампл Р., Шнайдерова М., Мардешич Т. (2011).«Антимюллеров гормон (АМГ) не только маркер для прогнозирования овариального резерва». Физиологические исследования / Academia Scientiarum Bohemoslovaca . 60 (2): 217–223. PMID 21114374.
- ↑ Деннис Н.А., Хоутон Л.А., Джонс Г.Т., ван Ридж А.М., Морган К., МакЛеннан И.С. (июль 2012 г.). «Уровень сывороточного антимюллерова гормона коррелирует со статусом витамина D у мужчин и женщин, но не у мальчиков». Журнал клинической эндокринологии и метаболизма . 97 (7): 2450–5. DOI: 10.1210 / jc.2012-1213. PMID 22508713.
- ↑ Фертильность: оценка и лечение людей с проблемами фертильности. Клиническое руководство NICE CG156 — Выпущено: февраль 2013 г.
- ↑ Илиодромити С., Келси Т.В., Ву О, Андерсон Р.А., Нельсон С.М. (2014). «Прогностическая точность антимюллерова гормона для живорождения после вспомогательного зачатия: систематический обзор и метаанализ литературы». Обновление репродукции человека . 20 (4): 560–570. DOI: 10,1093 / humupd / dmu003. PMID 24532220.
- ↑ Нельсон С.М., Йейтс Р.В., Флеминг Р. (сентябрь 2007 г.). «Сывороточный антимюллеров гормон и ФСГ: прогнозирование живорождения и экстремальных реакций в стимулированных циклах — значение для индивидуализации терапии». Репродукция человека . 22 (9): 2414–2421. DOI: 10.1093 / humrep / dem204. PMID 17636277.
- ↑ Нельсон С.М., Йейтс Р.В., Лайалл Х., Джеймисон М., Трейнор И., Гаудуан М., Митчелл П., Амброуз П., Флеминг Р. (апрель 2009 г.). «Основанный на антимюллеровом гормонах подход к контролируемой стимуляции яичников для вспомогательного зачатия». Репродукция человека . 24 (4): 867–875. DOI: 10,1093 / humrep / den480. PMID 19136673.
- ↑ Broer SL, Dólleman M, Opmeer BC, Fauser BC, Mol BW, Broekmans FJ (2011). «AMH и AFC как предикторы чрезмерного ответа при контролируемой гиперстимуляции яичников: метаанализ». Обновление репродукции человека . 17 (1): 46–54. DOI: 10.1093 / humupd / dmq034. PMID 20667894.
- ↑ Seifer DB, Maclaughlin DT (сентябрь 2007 г.). «Вещество, ингибирующее мюллериан, является новым клиническим фактором роста яичников». Фертильность и бесплодие . 88 (3): 539–46. DOI: 10.1016 / j.fertnstert.2007.02.014. PMID 17559842.
- ↑ Wallace WH, Kelsey TW (июль 2004 г.). «Яичниковый резерв и репродуктивный возраст могут быть определены путем измерения объема яичников с помощью трансвагинальной сонографии». Репродукция человека . 19 (7): 1612–7. DOI: 10,1093 / humrep / deh385. PMID 15205396.
- ↑ Cupisti S, Dittrich R, Mueller A, Strick R, Stiegler E, Binder H, Beckmann MW, Strissel P (декабрь 2007 г.). «Корреляция между антимюллеровым гормоном, ингибином B и активином A в фолликулярной жидкости у пациентов с ЭКО / ИКСИ для оценки созревания и потенциала развития ооцитов». Европейский журнал медицинских исследований . 12 (12): 604–8. PMID 18024272.
- ↑ Dewailly D, Lujan ME, Carmina E, Cedars MI, Laven J, Norman RJ, Escobar-Morreale HF (2013).«Определение и значение морфологии поликистозных яичников: отчет рабочей группы Общества синдрома избытка андрогенов и поликистозных яичников». Обновление репродукции человека . 20 (3): 334–352. DOI: 10.1093 / humupd / dmt061. PMID 24345633.
Frontiers | Антимюллеров гормон во время естественного цикла представляет значительные вариации внутри и между циклами при измерении с помощью полностью автоматизированного анализа
Введение
Антимюллеров гормон (АМГ) — это димерный гликопротеин, продуцируемый гранулезными клетками преантральных и малых антральных фолликулов в яичниках, и его производство не зависит от фолликулостимулирующего гормона (ФСГ) (1).Высвобождение АМГ из клеток гранулезы приводит к измеряемым уровням в сыворотке, и было показано, что эти концентрации пропорциональны количеству развивающихся фолликулов в яичниках (2). Таким образом, АМГ стал одним из наиболее важных косвенных клинических маркеров резерва яичников (3) и используется клиницистами для прогнозирования ответа яичников на гиперстимуляцию при ЭКО, облегчения консультирования пациентов и индивидуализации режимов стимуляции. Более того, недавняя публикация продемонстрировала сильную положительную, не зависящую от возраста взаимосвязь между уровнем АМГ и количеством эуплоидных бластоцист, полученных после циклов ЭКО / ИКСИ (4), а также с частотой выкидышей (5).
Хорошо известно, что сывороточный АМГ демонстрирует высокую межиндивидуальную вариабельность, в основном связанную с разным количеством антральных фолликулов в группах женщин одного возраста (2). Это также зависит от таких факторов, как использование гормональных контрацептивов, беременность, индекс массы тела, курение (6) и использование гонадотропинов для стимуляции яичников (7, 8). Сывороточный АМГ обычно считается надежным тестом, который можно измерить в любой день естественного цикла с минимальной индивидуальной вариабельностью (6, 9–13).Однако недавние публикации вызвали сомнения в надежности одного теста AMH, взятого ad-hoc в естественном цикле. Горкем и др. продемонстрировали, что уровни АМГ в сыворотке, по-видимому, выше во время фолликулярной фазы по сравнению с лютеиновой фазой у бесплодных женщин с нормальным, высоким и низким резервом яичников (14). Другие авторы описали важную вариабельность концентраций АМГ во время менструального цикла, которая была признана более высокой, чем колебания, ожидаемые только на основании анализа (15, 16).Более того, было высказано предположение, что у молодых женщин может быть модель колебаний внутри цикла, которая отличается от таковой у женщин старшего возраста (17). Также были выявлены циркадные колебания уровней АМГ в сыворотке крови (18).
Эти колебания АМГ в течение естественного цикла ранее приписывались аналитическим вариациям, вызванным различными условиями, используемыми для хранения образцов и / или методом анализа (19). Но теперь AMH можно анализировать с помощью полностью автоматизированных анализов AMH, которые обладают высокой чувствительностью и точностью, с широким линейным диапазоном (20), что позволяет более эффективно обрабатывать образцы и сокращать возможные процедурные ошибки (20–22).
В настоящее время широко распространено мнение, что единичное измерение АМГ является точным отражением овариального резерва пациентки, и врачи серьезно принимают этот результат во внимание при консультировании женщин по вопросам их репродуктивного здоровья. В свете недавних публикаций, демонстрирующих вариабельность AMH как на протяжении менструального цикла, так и между последовательными циклами, возникают вопросы относительно того, будет ли надежным единичное измерение AMH. Целью этого исследования было изучить уровни АМГ в сыворотке у здоровых женщин, ведущих велосипедный спорт, с использованием полностью автоматизированного анализа Elecsys AMH (Roche, для платформы Cobas 601 ) в определенные моменты времени естественного цикла и в краткосрочной перспективе. межцикловые вариации.
Материалы и методы
Субъекты
Двадцать два здоровых добровольца были включены в это исследование, которое проводилось с апреля по декабрь 2017 года в клинике IVIRMA в Абу-Даби. В исследование были включены женщины в возрасте от 18 до 38 лет, с регулярным менструальным циклом от 28 до 32 дней и ИМТ от 18 до 28 кг / м2. Критерии исключения включали следующие факторы: прием гормональных контрацептивов в течение как минимум 2 месяцев непосредственно перед началом исследования, беременность, кормление грудью и предыдущие состояния, которые могут отрицательно повлиять на резерв яичников (операция на яичниках, химиотерапия, облучение органов малого таза).В исследование не вошли добровольцы с бесплодием. Участники заполнили письменную анкету, включая характер менструального цикла, предыдущие беременности, роды и выкидыши, этническую принадлежность, курение и возможные критерии исключения. Они были проинформированы о методах, обработке образцов и целях исследования, и все они подписали информированное согласие.
Забор крови
Образцы крови были взяты путем венепункции в клинике с 8:00 до 14:00, после чего образцы немедленно отправили в лабораторию, расположенную в том же центре, для немедленной обработки и дальнейшего анализа.Во время естественного цикла образцы собирали на 2/3 день (AMH_01), 10 день (средняя фолликулярная фаза, AMH_MFP), день подъема ЛГ (AMH_LHR), средняя лютеиновая фаза (AMH_MLP) и 2/3 день последующей менструация (AMH_02). Всплеск ЛГ был определен для целей нашего исследования как начавшийся, когда концентрация ЛГ поднялась на 180% по сравнению с последним значением сыворотки, доступным у этого пациента, и продолжала расти после этого (23). Для этого контролировали уровень ЛГ, эстрадиола и прогестерона, начиная с 10 дня естественного цикла, а затем каждые 3 дня до тех пор, пока не был диагностирован всплеск ЛГ (24, 25).Лютеиновая фаза была подтверждена повышенным уровнем прогестерона в сыворотке (> 3 нг / мл) через 8 дней после всплеска ЛГ.
Каждый раз брали один образец крови объемом 5 мл. Кровь центрифугировали и сыворотку разделяли на две части: одну для анализа AMH и одну для анализа гонадотропинов и стероидных гормонов. Анализ на ФСГ, ЛГ, эстрадиол и прогестерон проводили с использованием конкурентного иммуноанализа, производимого Roche, на платформе Cobas 601 ® . Результаты для этих гормонов были получены и оценены в тот же день сбора крови.Образцы сыворотки на AMH были разделены на аликвоты, заморожены при -20 ° C в тот же день сбора и сохранены для анализа партии. Все образцы от каждого участника исследования были проанализированы в одинаковых условиях в один и тот же день с использованием автоматического анализа Elecsys ® AMH (для платформы Cobas 601, Roche ® ) в соответствии с инструкциями производителя. Ожидаемая погрешность анализа составляла <5%, как описано производителем; Коэффициент вариации между анализами и внутри анализа для автоматизированного анализа Elecsys ® AMH был равен 0.5–1,4 и 0,7–1,9% соответственно (26).
Статистический анализ
База данных исследований была создана для всех оцениваемых переменных. Данные экспорта были правильно анонимизированы и проанализированы с помощью SPSS 22.0.
Демографические переменные и гормональные показатели были суммированы со средним значением и стандартным отклонением. Чтобы описать гормоны и их динамику, мы каждый раз определяли среднее значение и стандартное отклонение и представляли его в виде диаграмм. Кроме того, мы выполнили полиномиальную интерполяцию для динамических значений и представили вариации со средней полиномиальной интерполяцией и полосой дисперсии.
значений AMH были представлены для динамического описания AMH с использованием 4-ступенчатой полиномиально-экспоненциальной интерполяции данных. Эта полиномиально-экспоненциальная интерполяция также использовалась для вменения недостающих данных (10 недостающих точек данных). Пациенты не были разделены на категории в соответствии с исходным AMH, поскольку ранее нельзя было предположить однородную вариабельность в кластерных группах.
Тест корреляции Пирсона был выполнен между значениями AMH и другими гормонами вместе с временными отметками, а кластерный анализ был проведен для корреляции между динамическими паттернами AMH и демографическими параметрами.Для оценки любых динамических паттернов AMH, связанных с демографическими параметрами, мы применили кластерный анализ по коэффициентам полинома AMH, которые были рассчитаны ранее. Статистически значимым считалось значение p 0,05.
Этическое разрешение
Исследование было одобрено внутренним этическим комитетом под номером REFA011 и зарегистрировано на сайте Clinical.trials.gov: NCT03106272.
Результаты
Всего было проанализировано 100 образцов от 22 женщин, средний возраст которых составил 30 лет.7 ± 4,11 года и ИМТ 23,2 ± 3,63 кг / м 2 (Таблица 1). Все образцы были проанализированы с помощью автоматического анализа Elecsys ® AMH для платформы Cobas 601 (Roche ® ).
Таблица 1 . Исходные характеристики участников.
Внутрицикловые и межцикловые вариации
Значения сывороточных концентраций АМГ, полученные во время различных фаз менструального цикла, показаны в Таблице 2, а колебания, представленные в уровнях АМГ для каждого участника, представлены на Рисунке 1.Для каждого участника было обнаружено значительное продольное колебание уровней АМГ, выраженное как коэффициент вариации (CV) внутри цикла 20,7%. Это было рассчитано для всех индивидуальных показаний за день цикла (CV = среднее значение 0,207 ± SD 0,143; [CI95: 0,148, 0,267]; тест Шапиро = 0,0016). Для этих вариаций не наблюдалось никакой картины колебаний.
Таблица 2 . Значения AMH, полученные каждый день измерения для всех 22 участников, включая среднее, минимальное и максимальное значение.
Рисунок 1 . Представление значений AMH с использованием полиномиально-экспоненциальной интерполяции данных для каждого пациента в каждый момент времени. AMH_01: день 2/3 цикла. AMH_MFP: 10 день цикла, средняя фолликулярная фаза. AMH_LHR: день подъема LH. AMH_MLP: 8-й день после подъема ЛГ, середина лютеиновой фазы. AMH_02: 2/3 день последующего цикла.
При сравнении результатов между 2/3 днями цикла в обоих последовательных циклах средняя абсолютная межцикловая вариация АМГ составила 0,75 нг / мл с диапазоном от 0.03 до 2,81 нг / мл. Межцикловый CV составлял 0,28 (CI95: 0,16-0,39; p <0,0001). Следовательно, у наших участниц наблюдалась 28% разница между значениями АМГ, измеренными на 2/3 день двух последовательных менструаций.
Среднее значение AMH, полученное в каждый день измерения для всех 22 участников, значительно варьируется в течение цикла, как показано данными в Таблице 2, а также на графике прямоугольной диаграммы (Рисунок 2), где колебания внутри цикла показаны межцикловые вариации.
Рисунок 2 . Коробчатая диаграмма значений AMH, полученных в каждый момент времени. Линия в середине поля, представляющая медианное значение AMH. Поле, представляющее 25 и 75% квартиль. Верхние усы простираются от петли до наибольшего значения не дальше 1,5 * IQR (межквартильный диапазон). Нижний ус простирается от петли до самого низкого значения. AMH_01: день 2/3 цикла. AMH_MFP: 10 день цикла, средняя фолликулярная фаза. AMH_LHR: день подъема LH. AMH_MLP: 8-й день после подъема ЛГ, середина лютеиновой фазы.AMH_02: 2/3 день последующего цикла.
Другие репродуктивные гормоны, связанные с изменчивостью АМГ.
Все значения гормонов для АМГ, ФСГ, ЛГ, эстрадиола и прогестерона показаны в таблице 3. Никакой корреляции между АМГ и ФСГ, эстрадиолом и прогестероном не наблюдалось ни при каких условиях. Однако была обнаружена значимая положительная корреляция между концентрациями LH_LHR и AMH ( t — значение: 5,962; p <0,0001).
Таблица 3 .Значения AMH, FSH, LH, E2 и P4, полученные каждый день измерения для всех 22 участников.
Обсуждение
Одним из преимуществ AMH по сравнению с другими показателями резерва яичников, такими как фолликулостимулирующий гормон (ФСГ), является то, что он, как считается, имеет минимальные вариации в течение менструального цикла, и, как результат, его можно тестировать в любой день цикл. Однако исследования, оценивающие стабильность уровней АМГ на протяжении менструального цикла, противоречивы и трудны для интерпретации из-за различий в используемых анализах.Настоящее исследование четко продемонстрировало статистически значимое изменение уровней АМГ в сыворотке крови с использованием полностью автоматизированного анализа АМГ во время спонтанного менструального цикла в группе здоровых женщин репродуктивного возраста. Этот результат согласуется с другими предыдущими исследованиями (27–30), некоторые из которых выявили особую закономерность изменения с максимальным уровнем АМГ в среднефолликулярной фазе, снижающимся во время овуляции с повторным повышением лютеиновой кислоты. фаза (16, 28, 29, 31). Было высказано предположение, что этот паттерн отражает роль АМГ в росте фолликулов (32).Текущий анализ показал, что женщины, независимо от их яичникового резерва, демонстрировали статистически значимые внутри- и межцикловые вариации АМГ, однако четкую картину колебаний выявить не удалось. Примечательно, что во время повышения уровня ЛГ наблюдалась значительная положительная ко-вариация между уровнями АМГ и ЛГ в сыворотке. Эта связь между уровнями ЛГ и АМГ была описана также Bungum et al. (18), когда они исследовали циркадные вариации сывороточного АМГ. Эта корреляция между обоими гормонами указывает на совместный регуляторный механизм между AMH и секрецией LH, что подтверждается недавним открытием рецепторов AMH в значительной подгруппе центральных нейронов GnRH у мышей и людей (33), что должно стимулировать дальнейшие исследования.
Для включенных женщин значения АМГ варьировали на 20,7% в течение всего цикла от первого анализа сыворотки, полученного в начале цикла, до 2/3 дня последующих менструаций. Эти колебания AMH более чем в три раза превышают ожидаемые значения, связанные с неточностью анализа (<5% ожидаемая погрешность анализа для автоматического анализа Elecsys ® AMH) и, следовательно, могут отражать биологические колебания. Внутрииндивидуальные вариации также были продемонстрированы с использованием различных тестов для анализа сыворотки (34).
На сегодняшний день данные о вариабельности АМГ в течение менструального цикла противоречивы (19). Некоторые из этих расхождений могут быть объяснены включением ановуляторных циклов, нечастого отбора проб крови, обработки образцов или вмешательства в анализ. В связи с этим настоящее исследование имеет несколько сильных сторон. Все образцы крови каждого испытуемого были проанализированы за один прогон в один и тот же день на одной платформе Cobas Elecsys, что снизило аналитическую изменчивость и искажающие факторы. В будущих исследованиях можно рассмотреть возможность повторения анализа образцов на отдельной платформе Cobas Elecsys для проверки качества.Еще одним важным преимуществом является то, что в среднем 4,5 образца на участника были проанализированы в течение естественного цикла, и овуляция была подтверждена путем измерения сывороточных концентраций ЛГ и прогестерона в лютеиновой фазе во всех циклах, что позволило избежать низкой точности анализов мочи для определения овуляции. Кроме того, в этом исследовании для анализа образцов использовался полностью автоматический анализ AMH, который, как ранее было показано, имеет низкую аналитическую вариабельность во всем диапазоне анализа (22, 35). Все образцы были получены утром или в начале дня, чтобы избежать возможных суточных колебаний (18).Однако количество участников нашего исследования ограничено.
Выявленные внутрицикловые вариации у здоровых женщин аналогичны данным, опубликованным Hadlow et al., Которые выявили средние внутрииндивидуальные вариации концентрации АМГ 20% (комбинированные аналитические и биологические) у бесплодных женщин с овуляторными циклами во время период обучения 3 цикла (16). Напротив, участники настоящего исследования представляют собой репрезентативную выборку женщин репродуктивного возраста с овуляторными циклами.Кроме того, значительные внутрииндивидуальные вариации были выявлены за более короткий период времени (один овуляторный цикл). Степень AMH-вариации в текущем анализе выше, чем ранее описанная Lambert-Messerlian, который пришел к выводу, что, несмотря на вариацию на 16% в течение всего цикла, сбор образцов может быть выполнен в любой день для оценки резерва яичников (15). Вариабельность более 20% при полностью автоматизированном анализе AMH в настоящем исследовании должна быть напоминанием клиницистам о том, что забор образцов AMH в любой день менструального цикла может не адекватно отражать истинный резерв яичников.
Очевидно, что уровни АМГ колеблются не только внутри циклов, но и между циклами. В настоящем исследовании была выявлена межцикловая вариабельность 28% ( p <0,0001) между 2 последовательными циклами. Кроме того, 4 участника с уровнем АМГ <1,2 нг / мл на 2/3 день первого цикла (AMH_01) были бы отнесены к категории имеющих низкий АМГ на основании Болонских критериев (36). Двое из этих четырех добровольцев показали нормальный уровень АМГ после повторной оценки на 2/3 день последовательного цикла (AMH_02).Эти различия в последовательных циклах могут быть отражением различий в количестве антральных фолликулов (AFC). Это также может отражать различный ответ яичников, который можно увидеть в клинической практике, несмотря на назначение одного и того же протокола лечения той же пациентке, но в другом цикле (37, 38). Это очень важный вывод, который может изменить текущую клиническую практику с точки зрения тестирования AMH. Межцикловая оценка сывороточного АМГ на 2/3 день, безусловно, заслуживает дальнейшего изучения.
В то время как реальный запас яичников может не изменяться в течение естественного цикла или между последовательными циклами, уровни АМГ в сыворотке изменяются из-за биологических вариаций и, кроме того, необычных изоформ АМГ, которые также были описаны (39).Ясно, что АМГ — молекула, которую нелегко определить количественно. Однако важные клинические решения часто основываются на одной случайной записи AMH, даже на дозе гонадотропинов, назначаемой в циклах ЭКО / ИКСИ (34).
Предыдущие публикации показали, что измерение АМГ, выполняемое в течение первых нескольких дней цикла, хорошо коррелирует с ответом яичников на стимуляцию (базальный АМГ) (7, 8). Кроме того, перед консультированием женщин относительно их репродуктивного здоровья и результатов стимуляции яичников рекомендуется комбинированная оценка сывороточного АМГ и ультразвуковой оценки количества антральных фолликулов (AFC) в первые дни менструального цикла (8, 40).Комбинируя оба маркера яичников, AMH и AFC на 1-3 день цикла, врачи смогут с большей точностью определить развивающиеся фолликулы, которые, как ожидается, будут расти дальше после гормональной стимуляции. Это позволит клиницистам назначать наиболее подходящую дозу гонадотропинов для стимуляции яичников в любом заданном цикле, предлагая еще более индивидуализированное лечение.
Таким образом, это исследование четко продемонстрировало значительные внутрицикловые и межцикловые вариации концентраций АМГ в сыворотке на протяжении естественных овуляторных циклов и между двумя последовательными менструациями с использованием полностью автоматизированного анализа АМГ.На основе этих
AMH (ANTİ-MÜLLERİAN HORMON)
AMH TESTİ VE DEĞERLENDİRİLMESİ
AMH (антимюллеров гормон) kadın ve erkek vücudunda bulunan glikoprotein yapısında bir maddedir.
Трансформирующий рост β (TGF-β) ailesinin bir üyesidir. Çeşitli fonksiyonları olmasına rağmen başlıca fonksiyonu cinsiyet farklılaşmasıdır. Исми де затен бурадан гельмектедир.«Антимюллеровский» келимесинин анлами: Müller karşıtı demektir. Müller kanalı (Paramezonefrik kanal) dişi fetusta tüp, rahim ve vajinanın oluşmasını sağlayan kanaldır.Döllenme ve gebelik sonucunda erkek fetus meydana gelirse testislerden антимюллеров гормон salgılanarak bu kanalın gelişmesini engeller. Яни erkeklerin Анна karnında gelişimi sırasında rahim, yumurtalık ве tüp gibi kadınlık organlarının gelişmemesini бу гормон sağlar. AMH’nin ismi bu görevinden esinlenerek konulmuştur. Мюллерово ингибирующее вещество (MIS) veya Мюллерово ингибирующее вещество (MIF) olarak da adlandırılır.
Müller kanalını ilk tarif eden bilim adamı: Johannes Peter Müller’dir.AMH Анне Карнында erkek bebeğin gelişimi süresince testis dokusundaki sertoli hücrelerinden salgılanarak müller kanalının gelişmesini engeller. Eğer anne karnındaki bebek dişi ise testis dokusu olmadığı için AMH bu şekilde salgılanamaz ve müller kanalı (rahim, rahim ağzı, tüp, vajinanın üst kısmı) gelişir.
Kadınlarda Anti-müllerian гормонun salgılanması anne karnında 36. haftada iken overlerde granülosa hücrelerinde başlar ве doğumdan sonra da menopoza girene kadar devam eder.Kadınlardaki AMH düzeyi erkeklere göre hayat boyunca daha düşük seyreder. Kadınlarda salgılanan AMH’nin görevi folikül seçimini düzenlenmesidir. Kadınlarda yumurtlama dönemi boyunca küçük preantral foliküller büyüyerek antral foliküllere dönüşür ве yumurtlama meydana gelir, bu aşamalardaki hızı ve seçiciliği AMH sağlar.
Kadınlarda AMH yumurtalıklarda (overde) bulunan foliküllerden salgılanır. Foliküller yumurta hücresi taşıyan keseciklerdir. Küçük foliküller yani çapı 6 mm’ye kadar olan primer ve preantral, антральный foliküllerin duvarındaki granülosa hücrelerinden AMH salgılanabilir.Büyük foliküllerde ве atreziye uğrayan foliküllerde AMH üretilmez. Kadınlarda doğumdan menopoza kadar AMH salgılanması devam eder.
AMH normal değeri kaç olmalı?
Aslında kadınlarda antimüllarian гормон нормальный kan değerinin ne kabul edilmesi gerektiği konusunda net bir görüş birliği olmasa da genel olarak 1-3 ng / dl arası (bazı araştirörmacılara) 1 нг / дл altındaki değerler по сравнению с резервинином azaldığını gösterir.AMH testi ne zaman ve nasıl yapılır?
AMH kadın ovulatuar siklusu (adet ve yumurtlama döngüsü) süresince ve farklı sikluslar arasında değişiklik göstermez.Яни адетин kaçıncı günü tahlil yapılırsa yapılsın benzer değerler elde edilir, bu nedenle diğer yumurtalık rezerv tahlilleri gibi adetin 3. günü bakılması şart değildir. Adet kanaması olan veya olmayan ее dönemde tahlil yapılabilir. Tahlilin aç veya tok karnına yapılması farketmez. AMH değeri ölçümü diğer kan tahlilleri ile aynı şekilde koldaki damarlardan alınan кан иле kısa süre içerisinde yapılabilmektedir.Gebelik (hamilelik) döneminde AMH değeri:
Gebelikte ve lohusalık döneminde AMH düzeylerinde önemli bir değişiklik saptanmamıştur, gebe olmayan kadınzerıdın.Ancak günümüzde gebeliğin takibinde veya yönetiminde AMH değerlerinin kullanım alanı yoktur.Kısırlık, Yumurtalık kapasitesi (over rezerzi) ve AMH:
AMH гормону kadınlarda başlıca yumurtalık kapasitesi (over rezervi) değerlendirilmesi amacılıyla kullanı. Burada amaç kadının gebe kalabilme için гормональный düzeyinin, yumurta oluşturabilme yeteneğinin yeterli olmasının araştırılması veya gebe kalabilmesi için ilaç veya tüp bebekngirngınörınıdaviler.AMH’nin над rezervi belirlenmesinde FSH, E2 (östrojen), İnhibin-B gibi гормонлара göre çok daha güvenilir olduğu tespit edilmiştir. FSH ile etkileşmesi yok denilecek kadar azdır. AMH değeri yumurtalıklardaki küçük antral folküllerin sayısı ile orantılıdır bu nedenle overlerdeki изначальный folikül havuzunu çok iyi yansıtır. Over rezervini belirleme açısından AMH’ye en yakın yöntem antral folikül sayımı gibi görünmektedir. Yaş ilerlemesi ile birlikte первобытный folikül sayısı ве AMH değeri giderek azalır, Menopozdan sonra tespit edilemeyecek seviyeye gelir.AMH’nin günümüzde diğer гормон testleri ölçümlerine göre dezavantajı nispeten daha pahalı olması ве ее hastanede yapılamamasıdır. İlerleyen zamanlarda maliyeti düşecektir ve yaygınlaşacaktır.АМГ hormonun kullanılabileceği diğer durumlar:
— Юмурталик kapasitesi (Over rezervi) değerlendirilmesinde
— Erken menopoz ве menopoz tanısında
— Bir kadının Каца yaşında menopoza gireceğinin önceden tespitinde
— Yumurtalıklarla ilgili бир ameliyat sonrası над hasarının tespiti amacıyla
— Kemoterapi veya radyoterapi sonrası over hasarının tespiti amacıyla
— Erken ve gecikmiş puberte tanısında
— Polikistik over tanısı (PKOS hastalarında AMH değeri 2-3 kat yüksektir.)
— Kısırlık tedavilerinde СУЮ riskini öngörmek amacıyla
— Kısırlık tedavisi в Tup Bebek tedavilerinde başarı şansını belirleyebilmek amacıyla (АМГ düzeyi yüksek Olan hastalarda Tup Bebek başarısı Дах FAZLA bulunmuştur)
-. Зернистые hücreli над tümörlerini tanısında в nükslerin belirlenmesinde
— Erkeklerde Сертоль hücreleri ve sperm üretim fonksiyonu hakkında bilgi almak amacıyla
— AMH’nin müllerian kanal ve bundan gelişen rahim (матка), rahim ağzı (serviks), tüp (туба) ve yumurtalık (оверлейдези геленис) ве bazı kanserlerin tedavisinde ileride kullanılabileceğini düşündürmektedir.Бу konuda araştırmalar yapılmaktadır.Yapılan bir araştırmada FSH ile ovulasyon indüksiyonu yapılan hastalada siklus boyunca AMH değerlerinde azalma olduğu izlenmiştir. (Normalde spontan sikluslarda AMH değeri değişmemesine karşın) (kaynak)
AMH düşüklüğünü yükseltmek ve tedavisi mümkün müdür?
Hastalar tarafından sık sorulan sorulardan birisidir. За rezervi Яни Юмурталик kapasitesi değerlendirmesinde kullanılan diğer hormonlar Gibi АМГ де yumurtalıkların kadının yaşının ilerlemesi ве diğer faktörlere bağlı olarak değişen kapasitesi hakkında Bilgi verir ве бу nedenle nasıl hastanın yalını gençleştirmek mümkün değilse бушель tür Hormon değerlerinin yükseltilmesi, düzeltilebilmesi mümkün değildir.Bu nedenle hastaların AMH veya FSH değerlerini düzeltmek amacıyla gereksiz bitkiler, otlar, çaylar, destek kürleri peşinde koşmaması, bunlarla vakit kaybetmemesi gerekir. Kısırlık tedavisinde vakit çok değerlidir, geçen aylar yıllar hastanın aleyhine işler. Bu nedenle gereksiz ve zararlı olabilecek önerilerle vakit kaybetmek yerine konunun uzmanı doktorlar tarafından öneriler tedavi seçenekleri vakit kaybetmeksizin uygulanmalıdır.Menopoz yaşını tahmin etmede AMH değeri:
Bu konuda yapılan bazı araştırmalar bir kadının menopoza kaç yaşında gireceğini tahmin etme konuscelanı(kaynak 1, kaynak 2)İlgili Konular:
— Yumurtalık Kapasitesi (Over Rezervi) Deleerlendirilmesi
— FSH Hormonu Yüksekliği
— Kısırlık (İnfertilılılılılılılı)
Bu sitedeki yazıların her hakkı saklıdır, izinsiz kullanılamaz: Yasal uyarıНизкий уровень антимюллерова гормона
автор: Ava
(Монреаль)Мне 27 лет, и я только что получил результаты уровня АМГ (антимюллерова гормона), равного 1.0. Мой день 3 ФСГ в норме. Мне сказали, что это означает, что я не буду выращивать хорошие яйца.
Я опустошена, я надеялась забеременеть и завести семью, но эта новость причинила мне столько горя. Есть ли у меня какая-то надежда, что натуральные средства увеличат количество яиц?Естественное лечение низкого уровня антимюллерова гормона
Антимюллеровский гормон вырабатывается фолликулами яичников, а уровни АМГ используются для измерения количества антральных фолликулов в яичниках.У женщин с более низким уровнем АМГ меньше фолликулов и меньше яиц.
Тест AMH используется все чаще, потому что уровни антимюллерова гормона существенно не меняются в течение менструального цикла и могут быть измерены в любое время в течение менструального цикла.
Низкие уровни обнаруживаются у пожилых женщин (старше 38 лет), тогда как более высокие уровни обнаруживаются у женщин с СПКЯ.
Нормальные уровни АМГ: 2,0? 6,8 нг / мл.Важно отметить, что женщина с низким уровнем АМГ может зачать ребенка естественным путем.
Этот тест используется для оценки потенциала фертильности в зависимости от ответа яичников во время лечения ЭКО.Поскольку уровни АМГ коррелируют с количеством фолликулов, этот тест является хорошим предиктором реакции яичников на цикл ЭКО. Женщины с низким уровнем АМГ с большей вероятностью будут иметь плохую реакцию со стороны яичников.
Женщины с недостаточным овариальным резервом могут многое делать естественным путем. Есть ряд важных витаминов, которые поддерживают здоровую овуляцию и помогают лечить плохую реакцию яичников.
Основными являются витамин C, E, L-аргинин и CoQ10. Набор Improve Egg Health Kit может помочь людям с низким резервом яичников и является отличным вспомогательным комплектом для тех женщин, которые отчаянно нуждаются в быстром улучшении своего уменьшенного резерва яичников.
Благословения плодородия!
Гормональный антимюллеров (AMH) | Speciale
Hormonul anti-Mullerian (AMH) este un гормон протеиновый ale carui roluri Principale sunt legate de diferentierea sexa n viata intrauterina si de Estimarea rezervei ovariene de foliculi la femeie.
Numit i ингибитор вещества / гормона / фактора Mullerian, AMH имеет сходную структурную структуру с ингибитором активности TGF-β (трансформирующий фактор роста β). AMH nu se află sub influența gonadotropinelor hipofizare.
ncepând de la pubertate, AMH este produs de celulele din granuloasa foliculilor antrali, aflai în faza precoce de creștere. Acești foliculi urmează a fi selecționați pentru își finaliza dezvoltarea către stadiul de folicul matur, Care va elibera ovocitul la ovulație.Pe măsură ce femeia se apropie de sfârșitul perioadei fertile, numărul de foliculi antrali scade i astfel se уменьшить și serică концентрации гормона антимюллерова. Din acest motiv, AMH poate fi folosit pentruterminaea cu acuratețe destul de bună a rezervei de foliculi ovarieni, подразумевается, что anselor pe care le mai are femeia de a rămâne gravidă.
S-a mai arătat că AMH ignă i recrutarea foliculilor primordiali, astfel încât o valoare scăzută a AMH la o femeieiferă poate sugera или rată mai mare de recrutare a foliculilor șiveaiza de la quick.Pornind de la această premisă, определенная область AMH поате оценка момента când o femeie va intra la menopauză. AMH acționează i prinercisea unui efect ингибитор asupra intrării foliculilor în faza finală de creștere, процесс, зависимый от стимулирующей области прин FSH; astfel, un AMH crescut împiedică selecția unui număr mare de foliculi de către FSH, protejând astfel rezerva ovariană.
După vârsta de 25 ani, nivelul AMH urmează o scădere lentă, континуал pe tot parcursul vieții fertile, până la menopauză.
Utilitatea dozării AMH ca marker al rezervei ovariene constă în posibilitatea de Estimare a anselor femeii de a rămâne gravidă (un AMH scăzut indică или rezervă foliculară redusă i deci anse mici de stable, cécitate mici de predusa, cis deci anse mici de statés, cécitate mici de statés, cécité mici de deluxe) oportunității de efectuare стимуляторы яичников (AMH scăzut este asociat cu un răspuns slab la tehnicile de FIV i necesitatea unor doze mai mari de gonadotropine). Totodată, AMH poate ajuta i la evalarea răspunsului ovarian in cadrul programmelor de Ferizare in vitro (o valoare scăzută a AMH constituie un predictor pentru un răspuns ovarian slab, în care se vă obține un numn).Nivelul AMH является точным bună i pentru predicția unui răspuns excesiv la optimulare ovariană i poate fi folosit și pentru minimizarea riscului de sindrom de hiperstimulare ovariană.
Нивелульный гормон антимюллериановый жоаке ун рол șи в патогенезе синдрома оварелор полихистис (СОП). Необычный аномальный биохимический элемент СОП может вызвать дефицит ароматических гормонов эстрогенов. Printre acțiunile AMH se numără i ignarea activității aromatazei, ceea ce ar putea contribui la excesul de androgeni al femeilor cu ovare polichistice.Așadar, nivelul crescut al AMH poate fi o caracteristică a femeilor cu SOP.
n timpul embriogenzei, AMH este secretat de celule Sertoli ale testiculelor fetale i acționează prin blocked dezvoltării ductelor Muller (ductelor Paramezonefrice) la embrionul de sex masculin. La femeie, absența AMH face la ductele Muller să nu regreseze ci să își continue dezvoltarea către formarea tractului genital feminin. Activitatea inadecvată a AMH в timpul vieții внутриутробном poate duce la stări de Intersexualitate, organe genitale ambigue sau criptorhidie.
Mai multe despre când și de ce ajungem bărbat sau femeie puteți citi aici.
La bărbat, producția de AMH de către testicule rămâne ridicată în timpul copilăriei, dar scade marcat în timpul pubertății și vieții vulte.
Valorile normale ale AMH для загара с содержанием 1-8 мкг / л жидкости после употребления удобрений или менее 0,4 мкг / л жидкости после менопаузы. О valoare peste 8 мкг / л poate sugera ovare polichistice, iar o valoare sub 0,4 мкг / л индика или резерва яичников mult diminuată.У AMH spre limita inferioară нормальный индикатор оплодотворения scăzută pe termen легкое, astfel că femeia ar trebui să încerce să conceptă mai devreme sau să ia în Thinkrare recoltarea inghețarea de ovule.
Spre deosebire de ali marki utili pentru definedarea rezervei ovariene (FSH și ингибина B), определенная область AMH poate fi efectuată независимая от ziua ciclului menstrual.
ntrucât nivelul AMH poate fi crescut la femeile cu ovare polichistice, sugerând în mod fals o feritate crescută, dozarea гормонулуи требует însoțită și de o ecografie intravaginală.
Deși majoritatea femeilor cu rezervă ovariană redusă nu au niciun factor de risc, definedarea AMH este Recomandată в специальном femeilor cu vârsta peste 35-40 ani, cu istoric familial de menopauză precoce, antecedente personale химиотерапия, boli autoimune.
Având în vedere capacitya de ignare a creșterii țesuturilor derivate din ductele Muller (uter, trompe uterine, treimea superioară a vaginului), AMH este studiat în tratamentul endometriozei, adenomiozeui și.
Ссылка:
Anti-Müller-Hormon — Антимюллеров гормон — qaz.wiki
Das Anti-Müllerian-Hormon ( AMH ), а также Müllerian-ignierendes Hormon (MIH) bekannt, ist ein Glykoproteinhormon, dasstrukturell mit Inhibin und Activin aus der Beta-superfamilie des versenicles der Wachstumsdifferenzierung und Follikulogenese liegt. Beim Menschen ist das Gen für AMH AMH auf Chromosom 19p 13.3, während das Gen AMHR2 für seinen Rezeptor auf Chromosom 12 kodiert.
AMH wird durch SOX9 in den Sertoli-Zellen des männlichen Fötus aktiviert. Seine Expression hemmt die Entwicklung des weiblichen Fortpflanzungstrakts oder der Müller-Gänge (paramesonephrische Gänge) im männlichen Embryo, wodurch die Entwicklung von Eileitern, Gebärmutter und oberer Vagina gestoppt wird. Die AMH-Expression ist für die Geschlechtsdifferenzierung zu einem bestimmten Zeitpunkt während der Entwicklung des Fötus entscheidend und scheint durch den Kernrezeptor SF-1, die Transkriptions-GATA-Faktorenchsdiffernenzdas, Das Geskriptions-GATA-Faktorenchus, Das Geschrén, das .Es wurde gezeigt, dass Mutationen sowohl im AMH-Gen als auch im AMH-Rezeptor vom Typ II die Persistenz von Müller-Derivaten bei Männern verursachen, die ansonsten normalerweise maskulinisiert sind.
AMH ist auch ein Produkt von Granulosazellen der preantralen und kleinen Antrumfollikel bei Frauen. Daher ist AMH nur bis zur Menopause im Eierstock vorhanden. Die Produktion von AMH регулирует Follikulogenese, находясь в Rekrutierung von Follikeln aus dem Ruhepool hemmt, um den dominanten Follikel auszuwählen, wonach die Produktion von AMH abnimmt.Als Produkt der Granulosazellen, die jedes Ei umhüllen und ihnen Energie liefern, kann AMH auch als molkularer Biomarker für die родственник Größe der Eierstockreserve dienen. Beim Menschen ist dies hilfreich, da die Anzahl der Zellen in der Follikelreserve verwendet werden kann, um den Zeitpunkt der Menopause vorherzusagen. Bei Rindern kann AMH zur Auswahl von Frauen in multi-ovulatorischen Embryotransferprogrammen verwendet werden, indem die Anzahl der zum Eisprung entwickelten Antrumfollikel vorhergesagt wird.AMH kann auch als Marker für Funktionsstörungen der Eierstöcke verwendet werden, beispielsweise bei Frauen mit polyzystischem Ovarialsyndrom (СПКЯ).
Struktur
АМГ — это димеры гликопротеина с молмассой 140 кДа. Das Molekül besteht aus zwei identityischen Untereinheiten, die durch Sulfidbrücken verbunden sind und durch das N-terminale Dimer (Pro-Region) und das C-terminale Dimer gekennzeichnet sind. AMH объединяет в себе тип-2-рецептор AMHR2, содержит тип-I-рецептор и фосфорилирует TGF-Beta-Signalweg.
Функция
Эмбриогенез
Bei männlichen Säugetieren verhindert AMH die Entwicklung der Müller-Gänge in die Gebärmutter und andere Müller-Strukturen. Der Effekt ist ipsateral, dh jeder Hoden unterdrückt die Müller’sche Entwicklung nur auf seiner eigenen Seite. Beim Menschen findet diese Aktion in den ersten 8 Schwangerschaftswochen statt. Wenn aus den Gonaden kein Hormon produziert wird, entwickeln sich automatisch die Müller-Gänge, während die Wolff-Gänge, die für männliche Fortpflanzungsteile verantwortlich sind, automatisch absterben.Die im Blut messbaren AMH-Mengen varieren je nach Alter und Geschlecht. AMH intergiert mit specifischen Rezeptoren auf den Oberflächen der Zellen von Zielgeweben (Anti-Müllerian-Hormonrezeptoren). Der bekannteste und spezifischste Effekt, der durch die AMH-Typ-II-Rezeptoren vermittelt wird, umfasst den programmierten Zelltod (Apoptose) des Zielgewebes (der fetalen Müller-Gänge).
Eierstock
AMH wird während der Fortpflanzungsjahre von Granulosazellen des Eierstocks exprimiert und grenzt die Bildung von Primärfollikeln durch Hemmung einer übermäßigen Follikelrekrutierung durch FSH.Die AMH-Expression ist im Rekrutierungsstadium der Follikulogenese am größten, in den preantralen und kleinen antralen Follikeln. Diese Expression nimmt ab, wenn sich Follikel entwickeln und in das Selektionsstadium eintreten, in dem die FSH-Expression zunimmt. Einige Behörden schlagen vor, dass dies ein Maß für bestimmte Aspekte der Eierstockfunktion ist, das bei der Beurteilung von Zuständen wie dem Syndrom der polyzystischen Eierstöcke und vorzeitigem Versagen der Eierstöcke.
Андере
Die AMH-Produktion durch die Sertoli-Zellen der Hoden bleibt während der gesamten Kindheit bei Männern hoch ,inkt jedoch während der Pubertät und im Erwachsenenalter auf ein niedriges Niveau.Es wurde gezeigt, dass AMH die Produktion von Sexualhormonenregiert, und eine Veränderung der AMH-Spiegel (Anstieg bei Frauen, Abfall bei Männern) kann bei bei beiden Geschlechtern zu Beginn der Pubertät führen. Es wurde auch festgestellt, dass funktionelle AMH-Rezeptoren in Neuronen im Gehirn embryonaler Mäuse exprimiert werden, und es wird angenommen, dass sie eine Rolle bei der sexuell dimorphen Gehirnentwickzlungen der der der der der der.
Патология
Bei Männern kann eine unzureichende embryonale AMH-Aktivität zum persistierenden Müllerian- Ductus-Syndrom (PMDS) führen, bei dem ein rudimentärer Uterus vorhanden ist und die Hoden normalersenktise nich. Das AMH-Gen ( AMH ) или Gen für seinen Rezeptor ( AMH-RII ) вызывает нормальное отклонение от нормы. AMH-Messungen sind auch bei der Bewertung der Hodenpräsenz und -funktion bei Säuglingen mit Intersexuellen Zuständen, mehrdeutigen Genitalien und Kryptorchismus weit verbreitet.
Eine in Nature Medicine veröffentlichte Studie fand einen Zusammenhang zwischen dem гормонеллен Ungleichgewicht im Mutterleib und dem Syndrom der polyzystischen Eierstöcke (PCOS), insbesondere der vorgeburtlichen Exposition gegenlüber-Anti-Müber. Für die Studie injizierten die Forscher schwangeren Mäusen AMH, so dass sie eine höhere Hormonkonzentration als normal hatten. In der Tat gebar sie Töchter, die später PCOS-ähnliche Tendenzen entwickelten. Dazu gehörten Probleme mit der Fruchtbarkeit, verzögerte Pubertät und unregelmäßiger Eisprung.Um dies umzukehren, verabreichten die Forscher den polyzystischen Mäusen ein IVF-Medikament namens Cetrorelix, wodurch die Symptome verschwanden. Diese Experimente sollten beim Menschen bestätigt werden, aber es könnte der erste Schritt sein, um die Beziehung zwischen dem polyzystischen Eierstock und dem Anti-Müller-Hormon zu verstehen.
Blutspiegel
Bei gesunden Frauen ist AMH bei der Geburt im Nabelschnurblut entweder nur nachweisbar oder nicht nachweisbar und zeigt einen deutlichen Anstieg im Alter von drei Monaten.Obwohl es noch nachweisbar ist, fällt es bis zum Alter von vier Jahren ab, bevor es bis zum Alter von acht Jahren linear ansteigt und von der Mitte der Kindheit bis zum frühen Erwachsenenalter ziemlich konstantänändert der ziemlich konstantänändert nühdicht nühtändert — es sign ändert nühdert — es sign. Der Anstieg während der Kindheit und Jugend spiegelt wahrscheinlich verschiedene Stadien der Follikelentwicklung шире. Ab dem 25. Lebensjahrinkt die AMH in den Wechseljahren auf nicht nachweisbare Werte.
Die Standardmessung von AMH после Generation II-Assay .Dies sollte die gleichen Werte wie der zuvor verwendete IBC-Assay ergeben, aber AMH-Werte aus dem zuvor verwendeten DSL-Assay sollten mit 1,39 multipliziert werden, um den aktuellen Standards zu entsprechen verde unterschrechen.
Schwache Hinweise deuten darauf hin, dass AMH aufgrund von Variationen über den Menstruationszyklus nur in der frühen Follikelphase gemessen werden sollte. Außerdeminken die AMH-Spiegel unter der gegenwärtigen Verwendung oraler Kontrazeptiva und dem gegenwärtigen Rauchen von Tabak.
Referenzbereiche
Referenzbereiche für Anti-Müllerian-Hormon, wie aus Referenzgruppen in den Vereinigten Staaten geschätzt, sind wie folgt:
фрауэн:
Alter Einheit Wert Jünger als 24 Monate нг / мл Weniger как 5 пмоль / л Weniger как 35 24 Monate bis 12 Jahre нг / мл Weniger как 10 пмоль / л Weniger als 70 13–45 Яхре нг / мл 1 бис 10 пмоль / л от 7 до 70 Мехр алс 45 Джахре нг / мл Weniger как 1 пмоль / л Weniger как 7 Заказчик:
Alter Einheit Wert Jünger als 24 Monate нг / мл 15 до 500 пмоль / л 100 до 3500 24 Monate bis 12 Jahre нг / мл 7 бис 240 пмоль / л от 50 до 1700 Mehr als 12 Jahre нг / мл 0,7 до 20 пмоль / л 5 до 140 AMH-Messungen sind möglicherweise weniger genau, wenn die zu messende Person einen Vitamin-D-Mangel hat.
- ↑ Шен WH, Мур CC, Икеда Y, Паркер KL, Ingraham HA (июнь 1994). «Ядерный рецептор стероидогенного фактора 1 регулирует ген ингибитора мюллерова вещества: связь с каскадом определения пола». Ячейка . 77 (5): 651–661. DOI: 10.1016 / 0092-8674 (94) -7. PMID 8205615.






 Пониженное содержание гормона является признаком патологии яичек врождённого характера, влиянием возраста или опухолях яичек.
Пониженное содержание гормона является признаком патологии яичек врождённого характера, влиянием возраста или опухолях яичек.
 4 нг/мл;
4 нг/мл;